题目内容
【题目】对甲烷和 CO2 的高效利用不仅能缓解大气变暖,而且对日益枯竭的石油资源也有一定的补充作用,甲烷临氧耦合 CO2 重整反应有:
反应(i):2CH4(g)+O2(g)2CO(g)+4H2(g) △ H=-71.4kJmol-1
反应(ii):CH4(g)+CO2(g)2CO(g)+2H2(g) △ H=+247.0 kJmol-1
(1)写出表示 CO 燃烧热的热化学方程式:_____。
(2)在两个体积均为 2L 的恒容密闭容器中,起始时按表中相应的量加入物质,在相同温度下进行反应(ii):CH4(g)+CO2(g)2CO(g)+2H2(g) (不发生其它反应),CO2的平衡转化率如表所示:
容器 | 起始物质的量(n) / mol | CO2的平衡转化率 | |||
CH4 | CO2 | CO | H2 | ||
Ⅰ | 0.1 | 0.1 | 0 | 0 | 50% |
Ⅱ | 0.1 | 0.1 | 0.2 | 0.2 | / |
①下列条件能说明反应达到平衡状态的是_____。
A.v正(CH4) =2v逆(CO)
B.容器内各物质的浓度满足c(CH4)·c(CO2)=c2(CO)·c2(H2)
C.容器内混合气体的总压强不再变化
D.容器内混合气体密度保持不变
②达到平衡时,容器Ⅰ、Ⅱ内 CO 的物质的量的关系满足:2n(CO)Ⅰ_____n(CO)Ⅱ(填“>”、“=”或“<”)
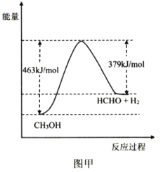
(3)将一定量的甲烷和氧气混合完成反应(i),其他条件相同,在甲、乙两种不同催化剂作用下, 相同时间内测得 CH4 转化率与温度变化关系如图所示。c 点_____(填“可能”、“一定”或“一定未”)达到平衡状态,理由是_____。

(4)CO2 也可通过催化加氢合成乙醇,其反应原理为:2CO2(g)+6H2(g)C2H5OH(g)+3H2O(g) H<0。设 m 为起始时的投料比,即 m= n(H2)/ n(CO2)。通过实验得到下列图象:
图1 图2
图2 图3
图3
①图 1 中投料比相同,温度从高到低的顺序为_________。
②图 2 中 m1、m2、m3 从大到小的顺序为_________。
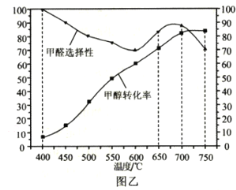
③图 3 表示在总压为 5 MPa 的恒压条件下,且 m=3 时,平衡状态时各物质的物质的量分数与温度的关系。T4 温度时,该反应压强平衡常数KP的计算式为_________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,代入数据,不用计算)。
【答案】CO(g)+![]() O2(g)=CO2(g) △ H=-282.7kJmol-1 C > 一定未 催化剂不会影响平衡转化率,在相同条件下,乙催化剂对应的 c 点的转化率没有甲催化剂对应的 b 点的转化率高,所以 c 点一定未平衡 T3>T2>T1 m1>m2>m3
O2(g)=CO2(g) △ H=-282.7kJmol-1 C > 一定未 催化剂不会影响平衡转化率,在相同条件下,乙催化剂对应的 c 点的转化率没有甲催化剂对应的 b 点的转化率高,所以 c 点一定未平衡 T3>T2>T1 m1>m2>m3 ![]()
【解析】
(1)书写燃烧热的热化学方程式,一定要保证:可燃物的化学计量系数为1;可燃物发生完全燃烧;生成产物是在常温常压下稳定存在的物质,根据盖斯定律可得:![]()
![]() ;
;
(2) ①A.2v正(CH4) =v逆(CO)时,反应才达到平衡状态,A项错误;
B.由于平衡常数未知,所以浓度满足上式不一定处于平衡状态,B项错误;
C.由于该反应是在恒温恒容条件下进行的,且属于非等体积反应,根据公式![]() 可知,当压强不变,该反应一定达到平衡,C项正确;
可知,当压强不变,该反应一定达到平衡,C项正确;
D.由于该反应是在恒温恒容条件下进行的,且全为气体参与,根据公式![]() 可知,密度恒定与平衡状态无关,D项错误;
可知,密度恒定与平衡状态无关,D项错误;
答案选C。
②构造容器Ⅲ:除起始物质只加入0.2molCH4和0.2molCO2外,其他条件与Ⅰ、Ⅱ相同;通过分析可知容器Ⅱ、Ⅲ中的平衡等效。容器Ⅲ相比于容器Ⅰ,进料增加了一倍,考虑到反应方程式,所以Ⅲ相比于Ⅰ,平衡逆移,CO的含量下降,所以2n(CO)Ⅰ>n(CO)Ⅱ;
(3)催化剂对于平衡无影响,相同条件下,加入甲催化剂达到的转化率b高于加入乙催化剂的转化率c,所以c点对应的一定不是平衡状态;
(4) ①由于该反应放热,所以温度越高反应物转化率越低,所以T3>T2>T1;
②对于两种反应物的反应,增加其中一种物质的投料,会使另一种物质的转化率提高,所以m1>m2>m3;
③由于投料按照化学计量系数比进行,所以反应任意时刻,n(H2):n(CO2)=3:1,且n(乙醇):n(水)=1:3;所以图中c线为H2,d线为CO2,a线为水,b线为乙醇;结合数据可知,T4时,平衡状态时,H2含量为0.375,CO2为0.125,水为0.375,乙醇为0.125。所以压强平衡常数的表达式为: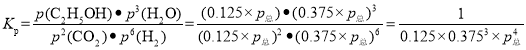 。
。

 阅读快车系列答案
阅读快车系列答案【题目】A~F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如下表所示。
元素 | 原子结构或性质 |
A | 原子最外层电子数是内层电子总数的1/5 |
B | 形成化合物种类最多的元素,其单质为固体 |
C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
D | 地壳中含量最多的元素 |
E | 与D同主族 |
F | 与E同周期,且最外层电子数等于电子层数 |
请回答下列问题:(用对应的化学用语回答)
(1)B在元素周期表中的位置是__________;用电子式表示A和E形成的化合物的形成过程 。
(2)A、 D 、E、 F离子半径由大到小的顺序为________________________________。
(3)C的某种氯化物的浓溶液可以腐蚀印刷电路板上的金属铜,此反应的离子方程式是__________________;
(4)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是____________________。该反应为 反应。(填“吸热”或“放热”)
(5)F的最高价氧化物与E的最高价氧化物的水化物反应的离子方程式为 。
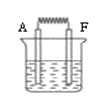
(6)如图:将A和F的单质与烧碱液构成原电池,负极的电极反应式为 ;外电路中电子从 电极流向 电极 。