题目内容
3.下列各组物质中,一定量的气体X和一定量的气体Y同时通入盛有溶液Z的洗气瓶中,最终肯定有沉淀生成的是(空气不参与反应)( )| A. | X-NO2 Y-SO2 Z-BaCl2 | B. | X-NH3 Y-SO2 Z-BaCl2 | ||
| C. | X-HCl Y-CO2 Z-Ca(OH)2 | D. | X-CO2 Y-SO2 Z-CaCl2 |
分析 A.二氧化氮和二氧化硫反应生成硝酸和硫酸,氯化钡和硫酸反应生成硫酸钡;
B.氨气和二氧化硫、水反应生成亚硫酸铵或亚硫酸氢铵,亚硫酸氢铵不能和氯化钡发生复分解反应;
C.少量二氧化碳与氢氧化钙反应生成碳酸钙沉淀,碳酸钙与盐酸反应生成氯化钙和二氧化碳和水;
D.二氧化硫、二氧化碳都是酸性氧化物,不和氯化钙反应.
解答 解;A.二氧化氮和二氧化硫反应生成硝酸和硫酸,氯化钡和硫酸反应生成硫酸钡,所以一定会产生沉淀,故A正确;
B.氨气极易溶于水生成氨水,氨水和二氧化硫反应生成亚硫酸铵,亚硫酸铵和氯化钡反应生成亚硫酸钡白色沉淀,若氨水和二氧化硫反应生成亚硫酸氢铵,不会和氯化钡反应生成沉淀,所以不一定有沉淀生成,故B错误;
C.少量二氧化碳与氢氧化钙反应生成碳酸钙沉淀,碳酸钙与盐酸反应生成氯化钙和二氧化碳和水,反应能否生成沉淀,取决于二氧化碳与氯化氢通入的量,故C错误;
D.二氧化硫、二氧化碳都是酸性氧化物,不和氯化钙反应生成沉淀,所以一定无沉淀生成,故D错误;
故选:A.
点评 本题考查了元素化合物的性质,明确物质性质和用量来判断产物是解本题关键,题目难度中等.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案
相关题目
14.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1L 1mol•L-1的两种强酸溶液中,所含氢离子数目均为NA | |
| B. | T℃时,1 L pH=6纯水中,含10-6NA个OH- | |
| C. | 1L浓度为1mol•L-1的Na2CO3溶液中含有NA个CO32- | |
| D. | 标准状况下22.4LHCl气体溶于水,其溶液中H+数为NA |
11.下列反应的离子方程式正确的是( )
| A. | 将NaOH固体加入热的浓NH4HSO3溶液中:NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| B. | 滴有稀硫酸的淀粉碘化钾溶液在空气中变蓝:2I-+O2+4H+═I2+2H2O | |
| C. | SO2使酸性KMnO4溶液褪色:5SO2+2MnO4-+2H2O═5SO42-+2Mn2++4H+ | |
| D. | 向次氯酸钙溶液中通入SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
18.实验室采购了部分化学药品.如图是从化学试剂商店买回的硫酸试剂标签上的部分内容.下列说法正确的是( )


| A. | 该硫酸的物质的浓度为9.2mol•L-1 | |
| B. | 1mol Al与足量的该硫酸反应产生3g氢气 | |
| C. | 配制200mL2.3mol•L-1的稀硫酸需量取该硫酸25mL | |
| D. | 打开浓硫酸的瓶盖,可以看到有白雾出现 |
15.下列选项中所涉及到的两个量一定不相等的是( )
| A. | 足量的钠在等物质的量的Cl2和O2中分别燃烧转移电子数 | |
| B. | 等物质的量的KO2与CaO2分别与水反应生成 的气体体积(相同条件下) | |
| C. | 100mL 1mol/L HNO3分别与1.4g Fe、2.8gFe完全反应时生成 的NO物质的量 | |
| D. | 等浓度等体积的盐酸、NaOH溶液分别与一定量Al反应生成等质量气体时转移的电子数 |
12.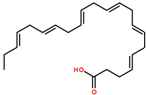 二十二碳六烯酸,俗称脑黄金,是一种对人体非常重要的不饱和脂肪酸,其结构简式如图.下列相关说法不正确的是( )
二十二碳六烯酸,俗称脑黄金,是一种对人体非常重要的不饱和脂肪酸,其结构简式如图.下列相关说法不正确的是( )
 二十二碳六烯酸,俗称脑黄金,是一种对人体非常重要的不饱和脂肪酸,其结构简式如图.下列相关说法不正确的是( )
二十二碳六烯酸,俗称脑黄金,是一种对人体非常重要的不饱和脂肪酸,其结构简式如图.下列相关说法不正确的是( )| A. | 该物质的分子式为:C22H32O2 | |
| B. | 该物质能使酸性高锰酸钾溶液褪色 | |
| C. | 该物质一定条件下能发生取代反应 | |
| D. | 1mol该物质最多能与7molBr2发生加成反应 |
13.津冀地区遭遇三轮雾霾袭击,非常简洁的描述灰霾天气,就是“细粒子气溶胶离子在高湿度条件下引发的低能见度事件”.气溶胶是胶体的一种,关于气溶胶,下列说法不正确的是( )
| A. | 气溶胶的分散剂是气体 | |
| B. | 根据分散质和分散剂的状态,可以将胶体分为9种 | |
| C. | 气溶胶分散质粒子直径在1nm-100nm | |
| D. | 胶体不能透过滤纸 |


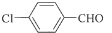 ;
; +3NaOH$\stackrel{高温高压}{→}$
+3NaOH$\stackrel{高温高压}{→}$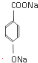 +NaCl+2H2O;
+NaCl+2H2O;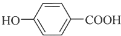 +(CH3)3COH $→_{△}^{浓H_{2}SO_{4}}$
+(CH3)3COH $→_{△}^{浓H_{2}SO_{4}}$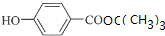 +H2O;
+H2O;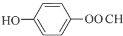 (任写一种结构简式).
(任写一种结构简式).