题目内容
8.如图是我国化学家近年来合成的两种聚乙炔衍生物分子的结构式.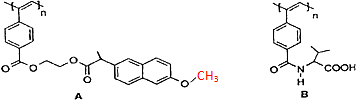
下列说法正确的是( )
| A. | A和B均能在一定条件下水解,且水解均生成两种产物 | |
| B. | A水解生成的高分子化合物中所有碳原子一定共面 | |
| C. | A和B的链节中均含有2个以上手性碳原子 | |
| D. | 1molA和B各与热碱液反应,均最多消耗2n mol NaOH |
分析 A.A物质含2n个-COOC-,B物质含n个-CONH-;
B.A水解的高分子化合物中碳原子不一定都共面;
C.A的链节中含有一个手性碳原子,B的链节中含有一个手性碳原子;
D.A中酯基水解生成的羧基能和NaOH反应,B中羧基和肽键水解生成的羧基能和氢氧化钠反应.
解答 解:A.A物质含2n个-COOC-,B物质含n个-CONH-,B水解生成两种产物,而A水解生成三种产物,除两种含苯环的物质还有乙二醇,故A错误;
B.A水解的高分子化合物中碳原子不一定都共面,因为聚乙炔基和苯环之间的共价键可以旋转,故B错误;
C.A的链节中含有一个手性碳原子,B的链节中含有一个手性碳原子,故C错误;
D.A中酯基水解生成的羧基能和NaOH反应,B中羧基和肽键水解生成的羧基能和氢氧化钠反应,所以1molA和B各与热碱液反应,均最多消耗2n mol NaOH,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,把握官能团及其性质关系是解本题关键,侧重考查酯、肽的性质,易错选项是B,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.下列说法正确的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | KI和HI中化学键类型完全相同 | |
| C. | Na2O2中既含有离子键又含有非极性共价键 | |
| D. | NH4Cl中只含有共价键 |
19.下列说法正确的是( )
| A. | 高分子化合物是纯净物 | |
| B. | 石油的裂化和煤的干馏属于化学变化,煤的液化属于物理变化 | |
| C. | 糖一定有甜味,有甜味的可能是糖 | |
| D. | 钠可以保存在十二烷中 |
16.下列关于物质用途的描述中错误的是( )
| A. | 钾钠合金可以用于快中子反应堆的热交换剂 | |
| B. | MgO是优质的耐高温材料 | |
| C. | 铝合金密度小、强度高,可制成汽车车轮骨架和飞机构件 | |
| D. | 用钠和氯气反应制备氯化钠 |
13.已知A为烃,B是烃的衍生物,由总物质的量为1mol的A和B组成的混合物在2.5mol氧气中完全燃烧,生成2mol二氧化碳和2mol水.A、B分子式不可能是下列组合中的( )
| A. | CH4O、C3H4O | B. | C2H4、C2H4O2 | C. | C3H6O3、CH2O2 | D. | C2H2、C2H6 |
20.2SO2(g)+O2(g)$\frac{\underline{\;V_{2}O_{5}\;}}{△}$2S03(g)是制备硫酸的重要反应之一.下列叙述正确的是( )
| A. | 催化剂V2O5,不改变该反应的逆反应速率 | |
| B. | 将2 mol SO2与2 mol O2放人密闭容器中,最终生成2mol SO3 | |
| C. | 在t1、t2时刻,SO2(g)的浓度分别是C1、C2,则时间间隔t1-t2内,SO2(g)消耗的平均速率为v=$\frac{{C}_{1}-{C}_{2}}{{t}_{2}-{t}_{1}}$ | |
| D. | 该反应是放热反应,则SO2的能量一定大于SO3的能量 |
17.下列物质中能与钠、氢氧化钠、碳酸氢钠都反应的是( )
| A. | 苯酚 | B. | CH3COOCH2CH2CH3 | C. | HCOOH | D. | CH3OH |
 如图所示是Zn和Cu形成的原电池,下列描述合理的是( )
如图所示是Zn和Cu形成的原电池,下列描述合理的是( )