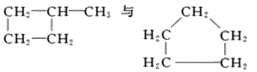��Ŀ����
����Ŀ��Ϊ�˺������û�ѧ�ܣ�ȷ����ȫ���������������Ҫ��ֿ��ǻ�ѧ��Ӧ�ķ�Ӧ�ȣ�����ȡ��Ӧ��ʩ����ѧ��Ӧ�ķ�Ӧ��ͨ����ʵ����вⶨ��Ҳ�ɽ����������㣮
��1��ʵ���ã�5g�״���CH3OH��Һ���������г��ȼ�����ɶ�����̼�����Һ̬ˮʱ�ͷų�113.5kJ�����������ʾ�״���ȼ���ȵ��Ȼ�ѧ����ʽΪ��__________��
��2���������������Ȼ�ѧ����ʽ����a______b��������������=������������
H2��g��+![]() O2��g��=H2O��g����H1=akJmol-1
O2��g��=H2O��g����H1=akJmol-1
H2��g��+![]() O2��g��=H2O��l����H2=bkJmol-1
O2��g��=H2O��l����H2=bkJmol-1
��3����1mol��̬������ij�ֹ��ۼ���Ҫ���յ������м��ܣ��ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̣��ڻ�ѧ��Ӧ�����У���ѧ����Ҫ�����������γɻ�ѧ���ֻ��ͷ�������
��ѧ�� | H-H | N-H | N��N |
����/kJmol-1 | 436 | 391 | 945 |
��֪��ӦN2��g��+3H2��g��=2NH3��g����H=akJmol-1���Ը��ݱ������м������ݹ���a��ֵ��____________��ע����+������-������
��4�����ݸ�˹���ɿ��Զ�ijЩ����ͨ��ʵ��ֱ�Ӳⶨ�Ļ�ѧ��Ӧ�ķ�Ӧ�Ƚ������㣮����ˮú���ϳɶ����ѵ�������Ӧ���£�
��2H2��g��+CO��g��=CH3OH��g������H=-90.8kJmol-1
��2CH3OH��g��=CH3OCH3��g��+H2O��g������H=-23.5kJmol-1
��CO��g��+H2O��g��=CO2��g��+H2��g������H=-41.3kJmol-1
�ܷ�Ӧ��3H2��g��+3CO��g��=CH3OCH3��g��+CO2��g������H=________________��
��5������β���ﺬ�е�NO������������ȼ��ȼ�յĸ�����������������Ӧ���£�N2��g��+O2��g��2NO��g����H��0����֪�÷�Ӧ��2 404�棬ƽ�ⳣ��K=64��10��4����ش�
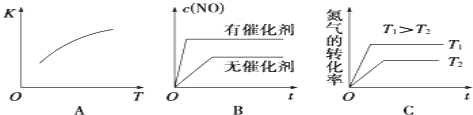
�ٽ�N2��O2�Ļ�����������º����ܱ������У���ͼ�仯������ȷ����_____������ĸ��ţ���
�ڸ��¶��£�ijʱ�̲��������N2��O2��NO��Ũ�ȷֱ�Ϊ2.5��10��1 mol/L��4.0��10��2 mol/L��3.0��10��3 mol/L����ʱ��Ӧ_______���������ڻ�ѧƽ��״̬������������Ӧ����������������淴Ӧ�������������������_______��
���𰸡�CH3OH��g��+![]() O2��g��=CO2��g��+2H2O��l�� ��H=-726.4KJ/mol �� -93 -246.4kJmol-1 AC ������Ӧ������� ��ΪQc=
O2��g��=CO2��g��+2H2O��l�� ��H=-726.4KJ/mol �� -93 -246.4kJmol-1 AC ������Ӧ������� ��ΪQc=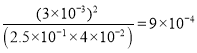 ��64��10��4�����Է�Ӧ������Ӧ�������
��64��10��4�����Է�Ӧ������Ӧ�������
��������
��1������5g�״���Ӧ�ų�����������1mol�״���Ӧ�ų���������д����ȷ���Ȼ�ѧ����ʽ��
��2����������ʽ��ˮ��״̬��ͬ������̬ˮ��ΪҺ̬ˮ�ų��������ݴ��жϣ�
��3��������H=��Ӧ����ܼ���-��������ܼ��ܽ��м��㣻
��4�����ݸ�˹���ɽ��м��㣻
��5�������¶ȡ������Է�Ӧ���ʺ�ƽ���ƶ���Ӱ������жϣ�
��1��5g�״���Ӧ�ų�������Ϊ113.5kJ�������32g�״���Ӧ�ų�������Ϊ726.4kJ���Ȼ�ѧ����ʽΪCH3OH��g��+![]() O2��g��=CO2��g��+2H2O��l�� ��H=-726.4KJ/mol��
O2��g��=CO2��g��+2H2O��l�� ��H=-726.4KJ/mol��
��2����������ʽ��ˮ��״̬��ͬ������̬ˮ��ΪҺ̬ˮ�ų�������b��Ӧ�ų���������a�࣬����a��b���Ǹ���������a��b��
��3����H=��Ӧ����ܼ���-��������ܼ���=945 kJ/mol+3��436 kJ/mol-2��3��391 kJ/mol
=-93 kJ/mol����a=- 93��
�ɸ�˹������2����+��+�ۣ���H=-90.8kJmol-1��2+��-23.5kJmol-1��+��-41.3kJmol-1��=-246.4 kJmol-1��
��5��A. ���ɷ�ӦN2��g��+O2��g��2NO��g����H��0����֪���÷�ӦΪ���ȷ�Ӧ�������¶�ƽ�����ƣ�Kֵ����A����ȷ��
B.��Ӧ�м����������Ӧ��������ƽ�ⲻ�ƶ���B�����
C.�¶����߷�Ӧ��������ƽ�����ƣ�������ת��������C����ȷ��
��ѡAC��
�� N2��g��+ O2��g�� 2NO��g����ijʱ��������N2��O2��NO��Ũ�ȷֱ�Ϊ2.5��10��1��4.0��10��2 ��3.0��10��3 mol/L��Qc=![]() ����K=64��10��4��Qc��K����֪ƽ�������ƶ���
����K=64��10��4��Qc��K����֪ƽ�������ƶ���

 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�����Ŀ��Ϊ�ﵽ����ʵ��Ŀ�ģ���Ӧ��ʵ�鷽���Լ���ؽ��;���ȷ����
ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� | ��ؽ��� |
A | ������ˮ��pH |
| pH��ֽ������ |
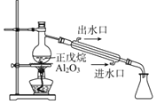
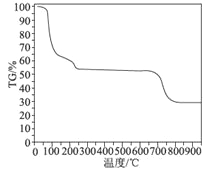
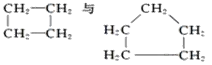
B | ̽��������C5H12���ѽ� |
| C5H12�ѽ�Ϊ���ӽ�С��������ϩ�� |
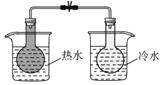
C | ʵ���¶ȶ�ƽ���ƶ���Ӱ�� |
| 2NO2 |
D | ��AlCl3��Һ�Ʊ�AlCl3���� |
| AlCl3�е�����ܼ�ˮ |
A.AB.BC.CD.D
����Ŀ�������������Ǵ�����Ⱦ��֮һ���û���̿��һ����̼��ԭ��������ɷ�ֹ������Ⱦ���ش��������⣺
��֪��2C(s)+O2(g)=2CO(g) ��H=-221 kJ/mol
C(s)+O2(g)=CO2(g) ��H=-393.5 kJ/mol
N2(g)+O2(g)=2NO(g) ��H=+181 kJ/mol
��1����ij��Ӧ��ƽ�ⳣ������ʽΪK=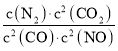 ����д���˷�Ӧ���Ȼ�ѧ����ʽ��_______�����д�ʩ�ܹ�����˷�Ӧ��NO��ת���ʵ��ǣ�����ĸ���ţ�____________��
����д���˷�Ӧ���Ȼ�ѧ����ʽ��_______�����д�ʩ�ܹ�����˷�Ӧ��NO��ת���ʵ��ǣ�����ĸ���ţ�____________��
a����������ѹǿ b�������¶� c��ʹ�����ʴ��� d������CO��Ũ��
��2�����ݻ�Ϊ2L���ܱ������м������̿(����)��NO��������ӦC(s)+2NO(g)![]() N2(g)+CO2(g)��NO��N2�����ʵ����仯���±���ʾ��
N2(g)+CO2(g)��NO��N2�����ʵ����仯���±���ʾ��
���ʵ���/mol | T1/�� | T2/�� | |||||
0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min | |
NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
��0��5min�ڣ���CO2��ʾ�ĸ÷�Ӧ����v(CO2)=______���������µ�ƽ�ⳣ��K=_____��
�ڵ�15 min���¶ȵ�����T2�����ݱ仯���ϱ���ʾ����T1_______T2������������������������������
����30minʱ������T2���䣬����������ټ�������ַ�Ӧ������2 mol�����ʱ��Ӧ_______�ƶ�������������
��3����ҵ�Ͽ����ð�ˮ��ȥ��ӦC(s)+2NO(g)![]() N2(g)+CO2(g)�в�����CO2���õ�NH4HCO3��Һ����ӦNH4++HCO3-+H2O
N2(g)+CO2(g)�в�����CO2���õ�NH4HCO3��Һ����ӦNH4++HCO3-+H2O![]() NH3��H2O+H2CO3��ƽ�ⳣ��K=____________������֪������NH3��H2O�ĵ���ƽ�ⳣ��Kb=2��10-5��H2CO3�ĵ���ƽ�ⳣ��Ka1=4��10-7��Ka2=4��10-11��ˮ�����ӻ�����Kw=1��10-14��
NH3��H2O+H2CO3��ƽ�ⳣ��K=____________������֪������NH3��H2O�ĵ���ƽ�ⳣ��Kb=2��10-5��H2CO3�ĵ���ƽ�ⳣ��Ka1=4��10-7��Ka2=4��10-11��ˮ�����ӻ�����Kw=1��10-14��