题目内容
15.用“>”或“<”填空:(1)酸性:H2CO3>H2SiO3
(2)碱性:Mg(OH)2>Al(OH)3.
(3)气态氢化物稳定性:H2O>H2S,
(4)还原性:H2S>HCl.
(5)氧化性Cu2+>Fe2+.
分析 (1)非金属性越强,对应最高价氧化物的水化物的酸性越强;
(2)金属性越强,对应最高价氧化物的水化物的碱性越强;
(3)非金属性越强,对应气态氢化物越稳定;
(4)非金属性越强,对应离子的还原性越弱;
(5)铁比铜活泼,则铁的还原性比铜强,则二价铁离子的氧化性比铜离子弱判断.
解答 解:(1)非金属性C>Si,对应最高价氧化物的水化物的酸性为H2SiO3<H2CO3,故答案为:>;
(2)金属性Mg>Al,对应最高价氧化物的水化物的碱性为Mg(OH)2>Al(OH)3,故答案为:>;
(3)非金属性Cl>S,对应气态氢化物为HCl>H2S,故答案为:>;
(4)非金属性Cl>S,对应离子的还原性为Cl-<S2-,故答案为:>;
(5)因为铁比铜活泼,则铁的还原性比铜强,则二价铁离子的氧化性比铜离子弱,故答案为:>.
点评 本题考查金属性和非金属性,明确物质的酸性、气态氢化物的稳定性,碱性与非金属性、金属性的关系是解答本题的关键,难度不大.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
5.将8g NaOH固体溶于水配成250mL溶液,从中取出50mL,则这50mL NaOH溶液的物质的量浓度为( )
| A. | 0.16 mol•L-1 | B. | 4mol•L-1 | C. | 0.8 mol•L-1 | D. | 8 mol•L-1 |
6.下列图①②③原子结构模型中依次符合卢瑟福、道尔顿、汤姆生的观点的是( )
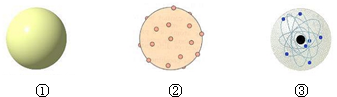

| A. | ①②③ | B. | ③①② | C. | ③②① | D. | ②①③ |
3.与Ne原子核外电子排布相同的一组离子是( )
| A. | Ca2+和Cl- | B. | F-与Na+ | C. | K+和Mg2+ | D. | Al3+和S2- |
3.某温度时,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中发生可逆反应生成气体Z,充分反应后X2的浓度为0.4mol/L,Y2的浓度为0.8mol/L,生成的Z的浓度为0.4mol/L,则该反应的化学方程式(Z用X、Y表示)是( )
| A. | X2+2Y2?2XY2 | B. | 2X2+Y2?2X2Y | C. | X2+3Y2?2XY3 | D. | 3X2+Y2?2X3Y |
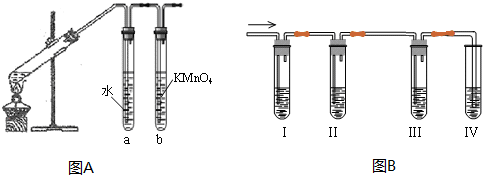
 金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如图所示:
金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如图所示: