��Ŀ����
����Ŀ��ij��ѧ��ȤС��������ͼװ���Ʊ��������������۲�����ɫ���ṩ��ѧҩƷ����м��ϡ���ᡢ����������Һ��
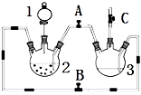
��1��ϡ����Ӧ���� ��(��д��������).
��2����ʵ��ͨ������A��B��C�������أ��������еĿ����ž����ٹرտ���B������A,�Ϳɹ۲쵽��������������ɫ���Է���ʵ�鿪ʼʱ�ž�װ���п���������
��3��ʵ��ʱΪ��ֹ����2������ͨ�����ܽ�������3�У��ɲ�ȡ�Ĵ�ʩ�� ��
��4����FeSO4��Һ�м���(NH4)2SO4������Ʊ�Ħ���ξ���[(NH4)2SO4��FeSO4��6H2O] (��Է�������392)���þ����һ���������ȶ������ױ�������������ˮ���������Ҵ���
��Ϊϴ��(NH4)2SO4��FeSO4��6H2O�ֲ�Ʒ�����з���������ʵ���
A������ˮϴ B��������ˮϴ��������ˮ�Ҵ�ϴ
C����30%���Ҵ���Һϴ D����90%���Ҵ���Һϴ
��Ϊ�˲ⶨ��Ʒ�Ĵ��ȣ���ȡa g��Ʒ����ˮ�����Ƴ�500mL��Һ����Ũ��Ϊc mol��L-1������KMnO4��Һ�ζ���ÿ����ȡ����Һ�����Ϊ25.00mL��ʵ������¼���£�
ʵ����� | ��һ�� | �ڶ��� | ������ |
���ĸ��������Һ���/mL | 25.52 | 25.02 | 24.98 |
i�ζ������з�����Ӧ�����ӷ���ʽΪ
ii�ζ��յ��������
iiiͨ��ʵ�����ݼ���ĸò�Ʒ����Ϊ (����ĸa��c��ʾ)���ϱ��е�һ��ʵ���м�¼�������Դ��ں����Σ���ԭ�������
A��ʵ�����ʱ���ӿ̶��߶�ȡ�ζ��յ�ʱ���Ը��������Һ�����
B���ζ�ǰ�ζ��ܼ��������ݣ��ζ�����������
C����һ�εζ��õ���ƿ�ô�װҺ��ϴ����������δ��ϴ
D�������Ը�����ر�Һ����ʱ��������в��ֱ��ʣ�Ũ�Ƚ���
���𰸡���1����Һ©����
��2����ֹ���ɵ�����������������
��3�������ۻ�������������
��4����D����i.MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O��ii.���һ�ε�������Һ����ɫ��Ϊdz��ɫ����30s����ɫ��iii.![]() ��100%��BC��
��100%��BC��
��������
�����������1����ʵ��Ŀ�����Ʊ���������������������ϡ���ᷴӦ�Ʊ������������˷�Ӧ��װ��2�н��У�ϡ��������Һ��Ӧʢ���ڷ�Һ©���У��ʴ�Ϊ����Һ©����
��2����B��C���ر�A������װ��2�в�������������װ��3�еĿ����ž���ʹװ�ô��ڻ�ԭ��Χ��Ȼ��ر�B����A����������ѹǿ���Ѳ�����FeSO4��ѹ�뵽װ��3�У�����Fe(OH)2��ɫ������������������Һ�������е�����������������������������������������ɫ�Ĺ۲�������ţ�����Ҫ�ų�װ���еĿ�������ֹ���ɵ��������������������ʴ�Ϊ����ֹ���ɵ�������������������
��3�������ۻ�����������������Է�ֹ����2������ͨ�����ܽ�������3�У��ʴ�Ϊ�������ۻ��������������
��4������Ϊ���������������ˮ���������Ҵ���Ӧ�����Ҵ�ϴ�ӣ�������������淋��ܽ⣬ͬʱ�����Ҵ���ˮ���ܣ��Ӷ��ﵽϴ�ӵ�Ҫ��ѡD���ʴ�Ϊ��D��
��i.���ø�����ص�ǿ�����ԣ�Fe2+��ǿ��ԭ�ԣ����߷���������ԭ��Ӧ��Fe2+��������Fe3+��1��Mn��+7����+2��5����С������5������ԭ�Ӹ���������غ㣬��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O���ʴ�Ϊ��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O��
ii.����Һ�еμ��и�����أ�����������Ϻ�ɫ����˵ζ����յ㣺���һ�ε��룬��Һ����ɫ��Ϊdz��ɫ����30s����ɫ���ʴ�Ϊ�����һ�ε��룬��Һ����ɫ��Ϊdz��ɫ����30s����ɫ��
iii.��Ϊ��һ����ڶ��Ρ����������ϴ��Բ��ƣ����ĸ��������Һ�����Ϊ![]() ml=25mL���������ӷ�Ӧ����ʽ���ó���n[(NH4)2SO4FeSO46H2O]=5n(KMnO4)=25��10-3��c��5mol����500mL��Һ�к���n[(NH4)2SO4FeSO46H2O]=25��10-3��c��5��500/25mol=2.5cmol��������������= 2.5c ��
ml=25mL���������ӷ�Ӧ����ʽ���ó���n[(NH4)2SO4FeSO46H2O]=5n(KMnO4)=25��10-3��c��5mol����500mL��Һ�к���n[(NH4)2SO4FeSO46H2O]=25��10-3��c��5��500/25mol=2.5cmol��������������= 2.5c �� ![]() �� 100% =
�� 100% = ![]() �� 100%��A�����Ӷ����������������ƫС���ʴ���B���ζ��ܼ��������ݣ��ζ����������ݣ������ĵ�Һ��������ӣ�����ȷ��C����ƿ�ô���Һ��ϴ������Һ�����ʵ������ӣ������ĸ�����ص�������ӣ�����ȷ��D�������Ը�����ر�Һ����ʱ��������в��ֱ��ʣ�Ũ�Ƚ��ͣ���ÿ�����ĵı�Һ���Ӧ��ȣ�������ɽϴ�ƫ���D���ʴ�Ϊ��
�� 100%��A�����Ӷ����������������ƫС���ʴ���B���ζ��ܼ��������ݣ��ζ����������ݣ������ĵ�Һ��������ӣ�����ȷ��C����ƿ�ô���Һ��ϴ������Һ�����ʵ������ӣ������ĸ�����ص�������ӣ�����ȷ��D�������Ը�����ر�Һ����ʱ��������в��ֱ��ʣ�Ũ�Ƚ��ͣ���ÿ�����ĵı�Һ���Ӧ��ȣ�������ɽϴ�ƫ���D���ʴ�Ϊ��![]() ��100%��BC��
��100%��BC��

����Ŀ�������������������ת����ϵ��ͼ��ʾ(���ַ�Ӧ�P��Ӧ��������ȥ����ͷ��ʾһ��ת��)�����и��������У���������ͼʾת����ϵ����
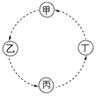
ѡ�� | �� | �� | �� | �� |
A |
| CH2=CH2 | CH2BrCH2Br | CH2OHCH2OH |
B | NaAlO2 | Al(OH)3 | Al2O3 | Al |
C | CH3CH2OH | CH3CHO | CH3COOH | CH3COOC2H5 |
D | SiO2 | H2SiO3 | Na2SiO3 | Si |
����Ŀ�������̿�����Ҫ��MnCO3��FeCO3��Al2O3��SiO2���Ʊ�MnSO4��H2O�Ĺ�������������
���������̿��м������ϡH2SO4�����ˣ�
��������Һ�м������MnO2�����ˣ�
����������ҺpH=a�����ˣ�
����Ũ�����ᾧ�����롢����õ���Ʒ��
���������Ʒ���ȡ�
��1���������У���������Ҫ�ɷ��� ��
��2����MnO2����Fe2+�����ӷ���ʽ����������
![]() MnO2 +
MnO2 +![]() Fe2++
Fe2++![]() ��
��![]() Mn2+ +
Mn2+ + ![]() Fe3+ +
Fe3+ +![]()
��3����ѡ��Cl2��Ϊ��������ȣ�MnO2��������Ҫ���ڣ�ԭ����Դ�㡢�ɱ��͡��ɱ������Ⱦ�� ��
��4����֪�������������������pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | |
��ʼ����ʱ | 3.4 | 6.3 | 1.5 | 7.6 |
��ȫ����ʱ | 4.7 | 8.3 | 2.8 | 10.2 |
ע���������ӵ���ʼŨ��Ϊ0.1mol/L
��������a��ȡֵ��Χ�� ��
��5����������ͨ���ⶨ��Ʒ����Ԫ�ص������������жϲ�Ʒ���ȡ�
��֪һ�������£�MnO4����Mn2+��Ӧ����MnO2 ��ȡx g��Ʒ�����Һ����0.1mol/L KMnO4��Һ�ζ�������KMnO4��Һy mL����Ʒ����Ԫ�ص���������Ϊ ��
����Ŀ����ѧ�о��빤ҵ�����г����õ���Һ�еķ�Ӧ��
��1��25��ʱ��0.05 mol��L��1Ba��OH��2��Һ��pH�� ������Ba��OH��2��Һ��pH��2��HCl��Һ��ϣ������û����ҺpH��7����Ba��OH��2��Һ��HCl��Һ�������Ϊ ��
��2��CO2��ת�����л���ʵ��̼ѭ����CO2![]() CH3OH
CH3OH![]() HCOOH����
HCOOH����
25 ��ʱ�������������ƽ�ⳣ��������
��ѧʽ | HCOOH | H2CO3 | HClO |
����ƽ�ⳣ�� | 1.7��10��4 | K1��4.3��10��7 K2��5.6��10��11 | 3.0��10��8 |
�ش��������⣺
�������ӷ���ʽ��ʾHCOONa��Һ�ʼ��Ե�ԭ�� ��
�����ʵ���Ũ����Ϊ0.1 mol��L��1�������������ʣ�
a��Na2CO3 b��NaClO c��HCOONa d��NaHCO3 ��pH�ɴ�С��˳���� ����������
��3�������£���0.2 mol��L��1��HCOOH��0.1 mol��L��1��NaOH��Һ�������ϣ�������Һ��pH��7��˵�����û����Һ��HCOOH�ĵ���̶� HCOONa��ˮ��̶�������������������������С��������
��4������Cr2O72-�ķ�ˮ���Խϴ�ij������ˮ�к�5.00��10��3 mol��L��1��Cr2O72-��Ϊʹ��ˮ�ܴ���ŷţ������´�����Cr2O72-![]() Cr3����Fe3��
Cr3����Fe3��![]() Cr��OH��3��Fe��OH��3����������ķ�ˮ�в�����c��Fe3������2��10��13 mol��L��1���������Cr3����Ũ��Ϊ mol��L��1 ����֪��Ksp[Fe��OH��3]��4.0��10��38��Ksp[Cr��OH��3]��6.0��10��31����
Cr��OH��3��Fe��OH��3����������ķ�ˮ�в�����c��Fe3������2��10��13 mol��L��1���������Cr3����Ũ��Ϊ mol��L��1 ����֪��Ksp[Fe��OH��3]��4.0��10��38��Ksp[Cr��OH��3]��6.0��10��31����