题目内容
下列各组中的三种酸,按酸性由强到弱的顺序排列的是( )
| A、H2SiO3,H2CO3,HNO3 |
| B、H2SO4,HClO4,HBrO4 |
| C、HNO3,H3PO4,H4SiO4 |
| D、H2SO4,H3PO4,HClO4 |
考点:非金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:非金属性越强,最高价氧化物对应水化物的酸性越强,以此来解答.
解答:
解:A.非金属性N>C>Si,则H2SiO3、H2CO3、HNO3酸性由弱到强,故A不选;
B.非金属性Cl的最强,HClO4的酸性最强,不能体现由强到弱的顺序,故B不选;
C.非金属性N>P>Si,则HNO3、H3PO4、H4SiO4的酸性由强到弱的顺序排列,故C选;
D.非金属性Cl>S>P,则H3PO4的酸性最弱,不能体现由强到弱的顺序,故D不选;
故选C.
B.非金属性Cl的最强,HClO4的酸性最强,不能体现由强到弱的顺序,故B不选;
C.非金属性N>P>Si,则HNO3、H3PO4、H4SiO4的酸性由强到弱的顺序排列,故C选;
D.非金属性Cl>S>P,则H3PO4的酸性最弱,不能体现由强到弱的顺序,故D不选;
故选C.
点评:本题考查非金属性的比较,为高频考点,把握同周期、同主族非金属性变化规律为解答的关键,侧重规律性知识的考查,注意高氯酸为含氧酸中酸性最强的酸,题目难度不大.

练习册系列答案
相关题目
下列关于钠、镁、铝性质说法正确的是( )
| A、铝的金属性最强 |
| B、镁的原子半径最大 |
| C、它们的最高价氧化物的水化物中,只有NaOH属于强碱 |
| D、铝的最高价是+3价,最低价是-5价 |
下列电子式的书写正确的是( )
A、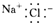 |
B、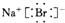 |
C、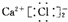 |
D、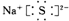 |
长周期元素周期表共有18个纵行,从左到右排为1~18列,即碱金属是第一列,稀有气体是第18列.按这种规定,下面说法不正确的是( )
| A、第9列元素中没有非金属 |
| B、第15列元素的原子最外层电子的排布是ns2np3 |
| C、最外层电子排布为ns2的元素都在第2列 |
| D、第10、11列元素分别处在d区和ds区 |
下列有关物质结构中的说法正确的是( )
| A、78 g Na2O2晶体中所含阴阳离子个数为4NA |
| B、1.5 g CH3+中含有的电子数为NA |
| C、3.4 g氨气中含有0.6NA个N-H键 |
| D、PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 |
如图是两种致癌物质的结构简式,以下的描述正确的是( )
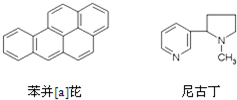

| A、它们都属于烃 |
| B、苯并[a]芘的分子式是C20H12 |
| C、尼古丁的分子式是C10H13N2 |
| D、苯并[a]芘的分子是由5个苯的结构单元并合而成,所以它是苯的同系物 |
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、常温常压下,100g98%硫酸溶液中含有的氧原子数为4NA |
| B、标准状况下,当活泼金属转移2NA个电子时,可从盐酸中置换产生44.8L H2 |
| C、15g CH3+中含有的电子数为0.8NA |
| D、1mol H2O2分子中非极性共价键数为NA |
把质量为m g的铜丝灼烧变黑,立即放入下列物质中,铜丝变红,而且质量仍为m g的是( )
| A、2-甲基-2-丙醇 | B、丙醇 |
| C、溴乙烷 | D、乙酸 |
 标准状况下,某同学向100mL H2S饱和溶液中通入SO2,所得溶液pH变化如图所示,下列分析中,正确的是( )
标准状况下,某同学向100mL H2S饱和溶液中通入SO2,所得溶液pH变化如图所示,下列分析中,正确的是( )| A、亚硫酸的酸性比氢硫酸的酸性弱 |
| B、ab段反应是:SO2+2H2S═3S↓+2H2O |
| C、原H2S溶液的物质的量浓度为0.05mol/L |
| D、b点对应的溶液导电性最强 |