题目内容
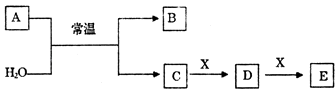
【题目】有机物A由碳、氢、氧三种元素组成。现取2.3 g A与2.8 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重2.2 g。回答下列问题:
(1)2.3 g A中所含氢原子、碳原子的物质的量分别是n(H)=______mol;n(C)=_______mol
(2)该有机物的分子式_____________,写出所有可能结构简式____________________。
【答案】 n(H)=0.3mol n(C)=0.1mol C2H6O CH3CH2OH或CH3OCH3
【解析】n(O2)=![]() =0.125mol,m(O2)=0.125mol×32g/mol=4g,根据质量守恒定律可得:m(有机物)+m(O2)=m(CO)+m(CO2)+m(H2O),则:m(CO)=2.3g+4g-2.7g-2.2g=1.4g,根据氧元素质量守恒可得2.3gA中O的质量等于产物中氧元素的总质量-氧气的质量=
=0.125mol,m(O2)=0.125mol×32g/mol=4g,根据质量守恒定律可得:m(有机物)+m(O2)=m(CO)+m(CO2)+m(H2O),则:m(CO)=2.3g+4g-2.7g-2.2g=1.4g,根据氧元素质量守恒可得2.3gA中O的质量等于产物中氧元素的总质量-氧气的质量=![]() ×16g/mol+
×16g/mol+![]() ×32g/mol+
×32g/mol+![]() ×16g/mol-4g=0.8g。
×16g/mol-4g=0.8g。
(1)2.3gA中:n(C)=![]() +
+![]() =0.1mol, n(H)=2n(H2O)=2×
=0.1mol, n(H)=2n(H2O)=2×![]() =0.3mol,答:2.3gA中所含氢原子、碳原子的物质的量各是0.3mol、0.1mol;
=0.3mol,答:2.3gA中所含氢原子、碳原子的物质的量各是0.3mol、0.1mol;
(2)2.3gA中:n(C)=0.1mol,n(H)=0.3mol,n(O)=![]() =0.05mol,所以2.3gA中C、H、O的原子个数比为0.1mol∶0.3mol∶0.05mol=2∶6∶1,则实验式为C2H6O,达到饱和,则分子式为C2H6O,对应的结构简式可能为CH3CH2OH、CH3OCH3,答:该有机物的分子式为C2H6O;可能的结构简式为CH3CH2OH、CH3OCH3。
=0.05mol,所以2.3gA中C、H、O的原子个数比为0.1mol∶0.3mol∶0.05mol=2∶6∶1,则实验式为C2H6O,达到饱和,则分子式为C2H6O,对应的结构简式可能为CH3CH2OH、CH3OCH3,答:该有机物的分子式为C2H6O;可能的结构简式为CH3CH2OH、CH3OCH3。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案