题目内容
某化学兴趣小组将下列装置按一定顺序连接后,在实验室中制取氯气并以氯气为原料制取无水FeCl3.已知FeCl3易潮解.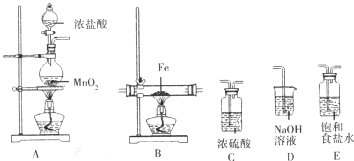
请回答下列问题:
(1)装置A中发生反应的离子方程式为
(2)各装置的正确连接顺序为(填装置的代号)A→
(3)B中反应开始前,需排除装置中的空气,应采取的方法是
(4)小明认为连接后的整套装置仍存在明显的缺点.为较好完成实验,则必须采取的改进措施是
(5)在实验中使用20mL12mol?L-1的浓盐酸与足量的MnO2反应,但生成Cl2总小于0. 06mol.试分析可能存在的原因:①
分析:(1)烧瓶A中反应4HCl(浓)+MnO2
MnCl2+Cl2↑+2H2O,反应本质为MnO2和氯离子在酸性条件下发生氧化还原反应;
(2)制备氯气中含有氯化氢和水蒸气,应先除氯化氢,后干燥,最后吸收尾气中未反应的氯气.氯化氢极易溶于饱和食盐水而氯气不易溶于水;
(3)先点A处酒精灯,使制取的Cl2排尽装置内的空气,防止铁被空气中氧气氧化;
(4)FeCl3易吸水潮解;
(5)盐酸变稀后与二氧化锰不再反应.
| ||
(2)制备氯气中含有氯化氢和水蒸气,应先除氯化氢,后干燥,最后吸收尾气中未反应的氯气.氯化氢极易溶于饱和食盐水而氯气不易溶于水;
(3)先点A处酒精灯,使制取的Cl2排尽装置内的空气,防止铁被空气中氧气氧化;
(4)FeCl3易吸水潮解;
(5)盐酸变稀后与二氧化锰不再反应.
解答:解:(1)烧瓶A中反应4HCl(浓)+MnO2
MnCl2+Cl2↑+2H2O,反应本质为MnO2和氯离子发生氧化还原反应,所以离子反应方程式为MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;
(2)制备氯气中含有氯化氢和水蒸气,除去氯化氢气体用饱和食盐水,除去水蒸气用浓硫酸,应先除氯化氢,后干燥,最后吸收尾气中未反应的氯气,防止污染空气,所以装置顺序为A→E→C→B→D,
浓盐酸有挥发性,所以氯气中含有氯化氢气体,氯化氢极易溶于水,氯气能溶于水,且与水反应,Cl2+H2O=H++Cl-+HClO,装置E中是饱和食盐水中的氯离子抑制氯气的溶解,降低氯气的溶解度,所以可用饱和食盐水除去氯气中混有的氯化氢气体,
故答案为:E;C;B;吸收氯气中的氯化氢气体;
(3)A处是制取氯气,B处是氯气和铁反应,所以先点A处酒精灯,使制取的Cl2排尽装置内的空气,防止铁被空气中氧气氧化,
故答案为:先点A处酒精灯,看到黄绿色气体充满装置B中,再加热装置B的反应管;
(4)已知FeCl3易吸水潮解,故需要在B和D之间连一个干燥装置,故答案为:在B和D之间连一个干燥装置;
(5)若20mL12mol?L-1的浓盐酸完全反应生成Cl20.06mol,但盐酸变稀后与二氧化锰不再反应,故生成Cl2总小于0.06mol,故答案为:盐酸变稀后与二氧化锰不再反应.
| ||
| ||
| ||
(2)制备氯气中含有氯化氢和水蒸气,除去氯化氢气体用饱和食盐水,除去水蒸气用浓硫酸,应先除氯化氢,后干燥,最后吸收尾气中未反应的氯气,防止污染空气,所以装置顺序为A→E→C→B→D,
浓盐酸有挥发性,所以氯气中含有氯化氢气体,氯化氢极易溶于水,氯气能溶于水,且与水反应,Cl2+H2O=H++Cl-+HClO,装置E中是饱和食盐水中的氯离子抑制氯气的溶解,降低氯气的溶解度,所以可用饱和食盐水除去氯气中混有的氯化氢气体,
故答案为:E;C;B;吸收氯气中的氯化氢气体;
(3)A处是制取氯气,B处是氯气和铁反应,所以先点A处酒精灯,使制取的Cl2排尽装置内的空气,防止铁被空气中氧气氧化,
故答案为:先点A处酒精灯,看到黄绿色气体充满装置B中,再加热装置B的反应管;
(4)已知FeCl3易吸水潮解,故需要在B和D之间连一个干燥装置,故答案为:在B和D之间连一个干燥装置;
(5)若20mL12mol?L-1的浓盐酸完全反应生成Cl20.06mol,但盐酸变稀后与二氧化锰不再反应,故生成Cl2总小于0.06mol,故答案为:盐酸变稀后与二氧化锰不再反应.
点评:本题以制取氯化铁粉末为载体,考查对实验方案设计评价,关键理清实验原理和目的及各装置的作用.题目综合性较强,题目难度中等.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
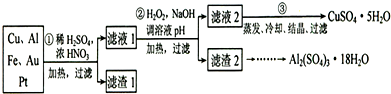
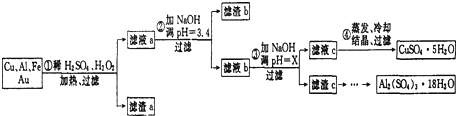
电子产品产生的大量电子垃圾对环境构成了极大的威胁.某化学兴趣小组将一批废弃的线路板简单处理后,得到含Cu、Al、Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
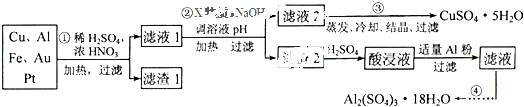
按要求回答下列问题:
(1)滤渣1中存在的金属有 .
(2)已知沉淀物的pH如下表:
①则操作②中X物质最好选用的是 (填编号)
a.酸性高锰酸钾溶液 b.漂白粉 c.氯气 d.双氧水
②理论上应控制溶液pH的范围是 .
(3)检验滤液2中既不存在Fe2+又不存在Fe3+的操作步骤是 .
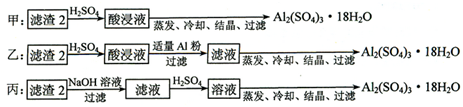
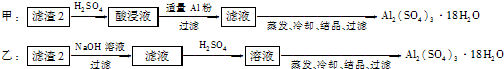
(4)用一个离子方程式表示在酸浸液中加入足量铝粉的反应: .
(5)由CuSO4?5H2O制备CuSO4时,应把CuSO4?5H2O放在 (填仪器名称)中加热脱水.
(6)现向一含有Ca2+、Cu2+的混合溶液中滴加Na2CO3溶液,若首先生成CuCO3沉淀,根据该实验可得出的结论是 (填序号)
A.Ksp(CuCO3)<Ksp(CaCO3) B.c(Cu2+)<c(Ca2+)
C.
>
D.
<
.

按要求回答下列问题:
(1)滤渣1中存在的金属有
(2)已知沉淀物的pH如下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.7 |
| Cu2+ | 4.9 | 6.7 |
| Al3+ | 3.0 | 4.4 |
a.酸性高锰酸钾溶液 b.漂白粉 c.氯气 d.双氧水
②理论上应控制溶液pH的范围是
(3)检验滤液2中既不存在Fe2+又不存在Fe3+的操作步骤是
(4)用一个离子方程式表示在酸浸液中加入足量铝粉的反应:
(5)由CuSO4?5H2O制备CuSO4时,应把CuSO4?5H2O放在
(6)现向一含有Ca2+、Cu2+的混合溶液中滴加Na2CO3溶液,若首先生成CuCO3沉淀,根据该实验可得出的结论是
A.Ksp(CuCO3)<Ksp(CaCO3) B.c(Cu2+)<c(Ca2+)
C.
| c(Cu2+) |
| c(Ca2+) |
| Ksp(CuCO3) |
| Ksp(CaCO3) |
| c(Cu2+) |
| c(Ca2+) |
| Ksp(CuCO3) |
| Ksp(CaCO3) |