��Ŀ����
����Ŀ��
��1������ʱ����IJ��������У��ձ����������� �� ��
��2������ʱ������ȷ�IJ���˳���ǣ���ĸ��ʾ��ÿ����ĸֻ����һ�Σ� ��
A����30mLˮϴ���ձ�2��3�Σ�ϴ��Һ��ע������ƿ����
B������ƽȷ��ȡ�����NaOH����������������ˮ��Լ30mL�����ò���������������ʹ�����ܽ�
C��������ȴ��NaOH��Һ�ز�����ע��250mL������ƿ��
D��������ƿ�ǽ����ߵ�ҡ��
E�����ý�ͷ�ιܼ�ˮ��ʹ��Һ����ǡ����̶�����
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1��2cm��
��3���������Ƶ���ҺŨ��ƫ�͵��� ��
A������NaOHʱ���������������
B��������ƿ��ת����Һʱ(ʵ�鲽��C)������Һ����������ƿ����
C��������ˮʱ���������˿̶���
D������ʱ���ӿ̶���
E������ǰ������ƿ������������ˮ
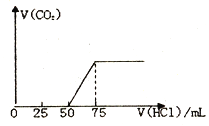
��4��ijͬѧ���ù���Na2CO3����Na2CO3��Һ�Ĺ�����ͼ��ʾ��������������� 

���𰸡���1�� 250 ml ����ƿ ��ͷ�ι� ��2�� BCAFED ��3�� ABC ��4�� �٢�
�������������������1������ʵ������IJ����Լ�ÿ��������Ҫ����ȷ����Ӧ��������������250mL��Һ����ѡ������ƿ�Ĺ��Ϊ250mL������ʱ�����м��㡢�������ܽ⡢��Һ��ϴ�ӡ����ݡ�ҡ�ȵȲ�����һ����������ƽ��������ҩ��ȡ��ҩƷ��NaOHӦ�����ձ��г��������ձ����ܽⲢ�ò��������裬��ȴ��ת�Ƶ�250mL����ƿ�У����ò���������������ˮ��Һ�����̶���1��2cmʱ�����ý�ͷ�ιܵμӣ�������Ҫ������Ϊ��ƽ��ҩ�ס��ձ���250mL����ƿ������������ͷ�ιܣ������������ձ���250mL����ƿ������������ͷ�ιܡ�
��2������ʵ�鲽���������֪��˳��ΪBCAFED
��3���������������ʵ����ʵ��������Һ�������Ӱ�죬����c=n/V������A������NaOHʱ��������������̣����ʵ��������٣�Ũ��ƫ�ͣ���ȷ��B��������ƿ��ת����Һʱ������Һ����������ƿ���棬���ʵ��������٣�Ũ��ƫ�ͣ���ȷ��C��������ˮʱ���������˿̶��ߣ���Һ���ƫ��Ũ��ƫ�ͣ���ȷ��D������ʱ���ӿ̶��ߣ���Һ���ƫС��Ũ��ƫ�ߣ�����E������ǰ������ƿ������������ˮ����Ӱ�죬Ũ�Ȳ��䣬����
��4��������Na2CO3ʱ��������������̣�������ʱ���ӿ̶��ߡ�

 ������ҵ����ν�����������ϵ�д�
������ҵ����ν�����������ϵ�д�����Ŀ�������йط�Ӧ�ȵ���������ȷ���ǣ� �� ����֪2H2��g��+O2��g���T2H2O��g����H=��483.6kJmol��1 �� ��������ȼ����Ϊ��H=��241.8kJmol��1
���ɵ���Aת��Ϊ����B��һ�����ȹ��̣��ɴ˿�֪����B�ȵ���A�ȶ�
��X��g��+Y��g���TZ��g��+W��s����H��0�����º��������´ﵽƽ������X��������Ӧ�ġ�H����
����֪��
���ۼ� | C��C | C�TC | C��H | H��H |
����/��kJmol��1�� | 348 | 610 | 413 | 436 |
�ϱ����ݿ��Լ���� ![]() ��g��+3H2��g����
��g��+3H2��g���� ![]() ��g���ķ�Ӧ�ȣ�
��g���ķ�Ӧ�ȣ�
���ɸ�˹���ɣ���֪����ͬ�����£����ʯ��ʯīȼ������1molCO2����ʱ���ų���������ȣ�
��25�棬101kPaʱ��1mol̼��ȫȼ������CO2���ų�������Ϊ̼��ȼ���ȣ�
A.�٢ڢۢ�
B.�ۢܢ�
C.�ܢ�
D.��