题目内容
5.下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题: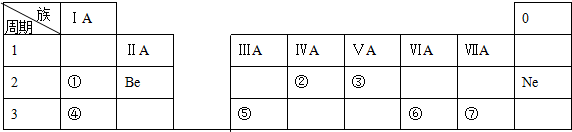
(1)⑦的元素符号是Cl
(2)②的原子结构示意图

(3)④和⑤分别对应的最高价氧化物的水化物的碱性强弱关系:④>⑤(填“>”或“<”);
(4)⑤的氧化物与⑥的最高价氧化物对应的水化物的稀溶液反应的离子方程式:Al2O3+6H+=3H2O+Al3+.
分析 由元素在周期表的位置可知,①为Li,②为C,③为N,④为Na,⑤为Al,⑥为S,⑦为Cl,据此结合各小题回答即可.
解答 解:由元素在周期表的位置可知,①为Li,②为C,③为N,④为Na,⑤为Al,⑥为S,⑦为Cl,
(1)⑦为Cl元素,故答案为:Cl;
(2)②为C元素,质子数为6,有2个电子层,最外层电子数为4,原子结构示意图为: ,故答案为:
,故答案为: ;
;
(3)元素的金属性越强,其对应最高价氧化物的水化物的碱性越强,由于金属性Na>Al,故碱性NaOH>Al(OH)3,故答案为:>;
(4)氧化铝与硫酸反应生成硫酸铝和水,氧化物不能拆,故离子反应方程式为:Al2O3+6H+=3H2O+2Al3+,故答案为:Al2O3+6H+=3H2O+2Al3+.
点评 本题考查位置结构与性质的关系及元素周期表和元素周期律,为高频考点,把握元素的位置分析元素为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
16.设NA表示阿伏加德罗常数,下列叙述中,正确的是( )
| A. | 在标准状况下,2.24 L二氧化硫与氧气混合气体中所含氧原子数为0.2 NA | |
| B. | 假设1mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为NA | |
| C. | 60g冰醋酸中,所含阴、阳离子总数为2NA | |
| D. | 标准状况下,3.36L乙烷中含有的非极性键数为1.05NA |
13.下列物质不能与Cl2反应的是( )
| A. | H2O | B. | NaOH溶液 | C. | Fe | D. | 浓H2SO4 |
20.下列化合物中,既含有共价键,又含有离子键的是( )
| A. | O2 | B. | CaO | C. | CH4 | D. | NaOH |
 .
. ,结构式是F-O-O-O-F.
,结构式是F-O-O-O-F. ;粒子E的名称是水合氢离子;粒子F对应的元素在周期表中的位置是第三周期、ⅢA族.
;粒子E的名称是水合氢离子;粒子F对应的元素在周期表中的位置是第三周期、ⅢA族.