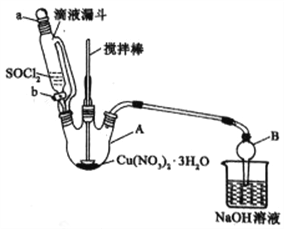
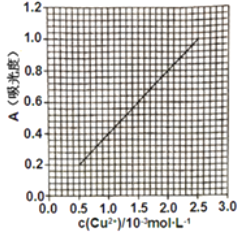
题目内容
【题目】NOx是造成大气污染的主要物质,现在工业上脱硝有多种方法。试回答下列问题
I.采用NaClO2溶液作为吸收剂可进行脱硝。反应一段时间后溶液中离子浓度的分析结果如下表:

写出NaClO2溶液和NO反应的脱硝过程中主要反应的离子方程式:______________________.
Ⅱ.用焦炭还原法将其转化为无污染的物质也可进行脱硝。已知:
2C(s)+O2(g)=2CO(g) △H1=-221.0kJ·mol-1;
N2(g)+O2(g)=2NO(g) △H2=+180.5kJ/mol
2NO(g)+2CO(g)=2CO2(g)+N2 (g) △H3=-746.0kJ /mol
回答下列问题
(1)用焦炭还原NO生成无污染气体的热化学方程式为______________________.
(2)在一定温度下,向甲、乙、丙三个恒容密闭容器中加入一定量的NO和足量的焦炭,反应过程中测得各容器中c(NO)(mo/L)随时间(s)的变化如下表:(已知:三个容器的反应温度分别为T甲=400℃、T乙=400℃、T丙=a℃)
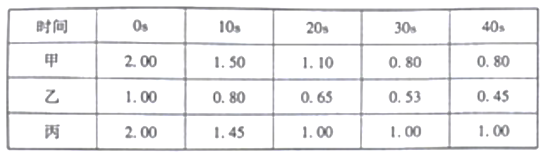
甲容器中,该反应的平衡常数K=_________丙容器的反应温度a__________400℃(填“>”,<”或“=”),理由是___________________________________.,用NH3催化还原NOx,也可以消除氮氧化物的污染。已知:8NH3(g)+6NO2(g)![]() 7N2(g)+12H2O(l),ΔH<0。相同条件下,在2L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间的变化如图所示
7N2(g)+12H2O(l),ΔH<0。相同条件下,在2L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间的变化如图所示
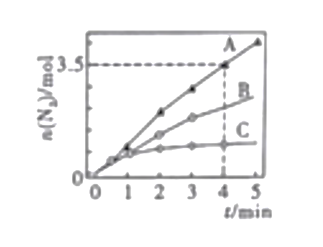
①在催化剂A的作用下0-4min的v(NO2)=___________________.
②该反应活化能Ea(A)、Ea(B)、Ea(C)由小到大的顺序是_____________,理由是_______________________________________.
③下列说法不正确的是____________(填序号)。
a.使用催化剂A达平衡时,△H值更大
b升高温度可使容器内气体颜色加深
c.单位时间内形成N-H键与O-H键的数目相等时,说明反应已经达到平衡
d.若在恒容绝热的密闭容器中反应,当平衡常数不变时,说明反应已经达到平衡
【答案】4NO+3ClO2-+4OH=4NO3-+2H2O+3Cl2NO(g)+C(s)![]() CO2(g)+N2(g) △H
CO2(g)+N2(g) △H![]() 573.75kJ/mol
573.75kJ/mol![]() (或0.5625)反应放热,甲、丙容器容积相同,反应起始量相同,达平衡时,K(丙)<K(甲)(或丙达平衡的时间比甲短)0.375mol/(L·min)Ea(A)<Ea(B)<Ea(C)相同时间内生成的N2越多,反应速率越快,活化能越低a
(或0.5625)反应放热,甲、丙容器容积相同,反应起始量相同,达平衡时,K(丙)<K(甲)(或丙达平衡的时间比甲短)0.375mol/(L·min)Ea(A)<Ea(B)<Ea(C)相同时间内生成的N2越多,反应速率越快,活化能越低a
【解析】
I.从题目表格中数据可以看出,产物中含有的离子主要是NO3-、Cl,则NaClO2溶液脱硝过程中主要反应的离子方程式为4NO+3ClO2-+4OH=4NO3-+2H2O+3Cl;
Ⅱ.(1)依据热化学方程式和盖斯定律计算得到所需热化学方程式;
(2)依据可逆反应2NO(g)+C(s)![]() CO2(g)+N2(g)在甲、乙、丙三种不同条件下建立平衡,建立三行式,找出平衡浓度,计算平衡常数;
CO2(g)+N2(g)在甲、乙、丙三种不同条件下建立平衡,建立三行式,找出平衡浓度,计算平衡常数;
依据可逆反应8NH3(g)+6NO2(g)![]() 7N2(g)+12H2O(l) ΔH<0,结合图像分析计算反应速率,比较活化能大小,判断平衡移动等。
7N2(g)+12H2O(l) ΔH<0,结合图像分析计算反应速率,比较活化能大小,判断平衡移动等。
I.从题目表格中数据可以看出,产物中含有的离子主要是NO3-、Cl,则NaClO2溶液脱硝过程中主要反应的离子方程式为4NO+3ClO2-+4OH=4NO3-+2H2O+3Cl,
因此,本题答案为:4NO+3ClO2-+4OH=4NO3-+2H2O+3Cl;
Ⅱ.(1)已知:
2C(s)+O2(g)=2CO(g) △H1=-221.0kJ·mol-1;
N2(g)+O2(g)=2NO(g) △H2=+180.5kJ/mol
2NO(g)+2CO(g)=2CO2(g)+N2 (g) △H3=-746.0kJ /mol
由盖斯定律(①+③-②)÷2得到反应的热化学方程式:2NO(g)+C(s)![]() CO2(g)+N2(g)
CO2(g)+N2(g) ![]() 573.75kJ/mol,
573.75kJ/mol,
因此,本题答案为:2NO(g)+C(s)![]() CO2(g)+N2(g)
CO2(g)+N2(g) ![]() 573.75kJ/mol;
573.75kJ/mol;
(2)甲容器中,30s时达到平衡:
2NO(g)+C(s)![]() CO2(g)+N2(g)
CO2(g)+N2(g)
起始浓度(mol/L)2.00 0 0
变化浓度(mol/L)1.20 0.60 0.60
平衡浓度(mol/L)0.80 0.60 0.60
平衡常数K=![]() =
=![]() =
=![]() ,
,
从表中数据可知,丙容器和甲容器起始量相同,丙达平衡的时间比甲短,说明丙反应比甲快,故温度比甲高,
因此,本题答案为:![]() (或0.5625); ;应放热,甲、丙容器容积相同,反应起始量相同,达平衡时,K(丙)<K(甲)(或丙达平衡的时间比甲短);
(或0.5625); ;应放热,甲、丙容器容积相同,反应起始量相同,达平衡时,K(丙)<K(甲)(或丙达平衡的时间比甲短);
①由图像可知,在催化剂A的作用下4min,n(N2)=3.5mol,则v(N2)=![]() =0.4375 mol/(L·min)
=0.4375 mol/(L·min)
由方程式8NH3(g)+6NO2(g)![]() 7N2(g)+12H2O(l),根据速率之比等于化学计量数之比,则
7N2(g)+12H2O(l),根据速率之比等于化学计量数之比,则
v(NO2)=![]() v(N2)=
v(N2)=![]() 0.4375 mol/(L·min)= 0.375mol/(L·min),
0.4375 mol/(L·min)= 0.375mol/(L·min),
② 由图像可知,相同时间内生成的N2的物质的量A>B>C,相同时间内生成的N2越多,说明反应速率越快,则活化能越低,该反应活化能Ea(A)、Ea(B)、Ea(C)由小到大的顺序是Ea(A)<Ea(B)<Ea(C),
因此,本题答案为:Ea(A)<Ea(B)<Ea(C);相同时间内生成的N2越多,反应速率越快,活化能越低;
③ a.△H值大小与是否使用催化剂无关,故a错误;
b.正反应为放热反应,升高温度平衡逆向移动,NO2浓度增大,容器内气体颜色加深,故b正确;
c.单位时间内形成N-H键与O-H键的数目相等时,即单位时间内生成8个NH3,同时生成12个H2O时,说明正逆反应速率相等,反应已经达到平衡,故c正确;
d.平衡常数只与温度有关,当平衡常数不变时,说明温度不变,说明反应已经达到平衡,故d正确。
因此,本题答案为:a。