题目内容
17.下列与有机物有关的化学用语不恰当的是( )| A. | 乙烯的比例模型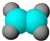 | B. | 1,3-丁二烯的键线式: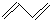 | ||
| C. | 甲基的电子式: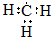 | D. | 乙醚的结构简式:CH3OCH3 |
分析 A.比例模型主要体现的是组成该分子的原子间的相对体积大小;
B.1,3-丁二烯分子中中含有两个碳碳双键,键线式的表示方法为:将碳、氢元素符号省略,只表示分子中键的连接情况,每个拐点或终点均表示有1个碳原子;
C.甲基为中性原子团,含有3个碳氢键,碳原子最外层为7个电子;
D.CH3OCH3为二甲醚,乙醚分子中含有4个碳原子.
解答 解:A.乙烯分子为平面结构,碳原子相对体积大于H原子,乙烯分子的比例模型为: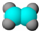 ,故A正确;
,故A正确;
B.1,3-丁二烯中含有2个C=C键,键线式中可以将碳氢键省略,其键线式为: ,故B正确;
,故B正确;
C.甲基中含有3个碳氢键,碳原子的最外层为7个电子,甲基的电子式为: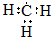 ,故C正确;
,故C正确;
D.两分子乙醇分子间脱水可以生成乙醚,乙醚的结构简式为:CH3CH2OCH2CH3,故D错误;
故选D.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,注意掌握比例模型、键线式、电子对、结构简式等化学用语的概念及书写原则,明确比例模型与球棍模型、结构简式与结构式的区别,试题侧重考查学生的规范答题能力.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
7. 决定物质性质的重要因素是物质结构.请回答下列问题:
决定物质性质的重要因素是物质结构.请回答下列问题:
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表所示:
A通常显+3价,A的电负性>B的电负性(填“>”、“<”或“=”);
(2)紫外光的光子所具有的能量约为399kJ•mol-1.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因紫外光具有的能量比蛋白质分子中主要化学键C-C、C-N、C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子;组成蛋白质的最简单的氨基酸中的碳原子杂化类型是sp2、sp3;
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),已知3种离子晶体的晶格能数据如表:
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:TiN>MgO>CaO>KCl;
其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有12个;
(4)[LiC60]PF6与NaCl具有类似的晶胞结构([LiC60]+表示1个Li+位于1个C60内部).[LiC60]PF6晶体中包含的化学键有BCD(填字母);
A.金属键 B.离子键 C.极性键 D.非极性键 E.范德华力
已知[LiC60]PF6晶体晶胞边长为a nm,计算[LiC60]PF6晶体的密度为$\frac{3488}{(a×1{0}^{-7})^{3}{N}_{A}}$g/cm3(用含a、NA的式子表示).
 决定物质性质的重要因素是物质结构.请回答下列问题:
决定物质性质的重要因素是物质结构.请回答下列问题:(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表所示:
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)紫外光的光子所具有的能量约为399kJ•mol-1.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因紫外光具有的能量比蛋白质分子中主要化学键C-C、C-N、C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子;组成蛋白质的最简单的氨基酸中的碳原子杂化类型是sp2、sp3;
| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有12个;
(4)[LiC60]PF6与NaCl具有类似的晶胞结构([LiC60]+表示1个Li+位于1个C60内部).[LiC60]PF6晶体中包含的化学键有BCD(填字母);
A.金属键 B.离子键 C.极性键 D.非极性键 E.范德华力
已知[LiC60]PF6晶体晶胞边长为a nm,计算[LiC60]PF6晶体的密度为$\frac{3488}{(a×1{0}^{-7})^{3}{N}_{A}}$g/cm3(用含a、NA的式子表示).
8.1mol乙烷在光照条件下,最多可以与多少摩尔的Cl2发生取代反应( )
| A. | 4mol | B. | 8mol | C. | 2mol | D. | 6mol |
5.某有机物的结构简式为 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )
 ,下列关于该有机物的叙述不正确的是( )
,下列关于该有机物的叙述不正确的是( )| A. | 能与金属钠发生反应并放出氢气 | |
| B. | 能在催化剂作用下与H2发生加成反应 | |
| C. | 不能氧化成醛 | |
| D. | 在浓H2SO4催化下能与乙酸发生酯化反应 |
12.下列实验操作与预期实验目的或所得实验结论一致的是( )
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时间后过滤 | 除去MgCl2溶液中少量FeCl3 |
| B | 向某溶液中加入BaCl2溶液生成白色沉淀,继续加稀硝酸沉淀不消失 | 证明溶液中含SO42- |
| C | 向某溶液中加入稀盐酸,放出无色无味气体,将气体通入澄清石灰水,石灰水变浑浊 | 证明该溶液中存在CO32- |
| D | 两支试管中装有等体积、等浓度的H2O2溶液,向其中一支试管中加入FeCl3溶液 | FeCl3溶液对H2O2分解速率无影响 |
| A. | A | B. | B | C. | C | D. | D |
2.写出下列基团的名称:
| -C═C- | ─C≡C─ | ─CH3 | ─CH2CH3或─C2H5 |
| 双键 | 三键 | 甲基 | 乙基 |
| ─OH | -COO-R | ─CHO | ─COOH |
| 羟基 | 醛基 | 酯基 | 羧基 |
6.质谱图表明某有机物的相对分子质量为70,红外光谱表征到C=C和C=O的存在,1H核磁共振谱如图(峰面积之比依次为1:1:1:3),下列说法正确的是( )
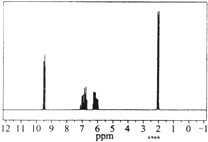

| A. | 分子中共有5种化学环境不同的氢原子 | |
| B. | 该有机物的结构简式为CH3CH=CHCOOH | |
| C. | 该物质的分子式为C4H6O | |
| D. | 该有机物不可能与氢气反应 |
8.3-苯基丙酸属于芳香酯的同分异构体共有多少种?( )
| A. | 22 | B. | 23 | C. | 24 | D. | 25 |