题目内容
6.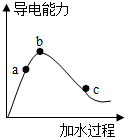 在一定温度下,冰醋酸(即纯醋酸)加水稀释过程中,溶液的导电能力如图所示,则:
在一定温度下,冰醋酸(即纯醋酸)加水稀释过程中,溶液的导电能力如图所示,则:(1)“O”点导电能力为0的理由是无自由移动的离子.
(2)用湿润的pH试纸测量a处溶液的pH,测量结果偏小(偏大、偏小或不变)
(3)比较a、b、c三点的下列数据大小或等量关系:(如a>b>c、c=a>b、a=b=c等)
①pH:c>a>b;
②醋酸的电离度:c>b>a;
③醋酸的电离平衡常数:a=b=c;
④a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:a=b=c.
(4)若使c点溶液中c(CH3COO-)增大,c(H+)减小,可采用的措施有(答二类不同的物质):
①加NaOH②加Na2CO3等固体.
(5)在稀释过程中,随着c(CH3COOH)的降低,下列始终保持增大趋势的量是BD.
A.c(H+) B.H+个数 C.CH3COOH个数 D.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$.
分析 (1)溶液的导电性与离子浓度有关,离子浓度越大,导电性越强;
(2)用湿润的pH试纸测量a处溶液的pH,相对于将溶液稀释;
(3)①导电能力越强,离子浓度越大,氢离子浓度越大,pH越小;
②溶液越稀,越促进醋酸电离;
③弱电解质的电离平衡常数只受温度影响,温度不变,电离平衡常数不变;
④abc三点醋酸浓度不同,但所含醋酸的物质的量相同;
(4)若使c点溶液中的c(CH3COO-)增大,可以采用升高温度、加入含有醋酸根离子的可能性盐、加入固体碱或加入和氢离子反应的固体物质,使c(H+)减小,可以加碱或加入和氢离子反应的固体物质;
(5)加水稀释,促进电离,n(CH3COO-)、n(H+)增大,但浓度减小,以此解答.
解答 解:(1)溶液的导电性与离子浓度有关,离子浓度越大,导电性越强,冰醋酸中没有自由移动的离子,所以冰醋酸不导电,故答案为:无自由移动的离子;
(2)据图可知将a处醋酸稀释,氢离子浓度增大,所以用湿润的pH试纸测量a处溶液的pH,测量结果偏小,故答案为:偏小;
(3)①导电能力越强,离子浓度越大,氢离子浓度越大,pH越小,则a、b、c三点溶液的pH为c>a>b,故答案为:c>a>b;
②溶液越稀,越促进醋酸电离,醋酸的电离度由大到小的顺序为c>b>a,故答案为:c>b>a;
③弱电解质的电离平衡常数只受温度影响,温度不变,电离平衡常数不变,所以abc三点的电离平衡常数相等,故答案为:a=b=c;
④abc三点醋酸浓度不同,但所含醋酸的物质的量相同,所以a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积相同,故答案为:a=b=c;
(4)若使c点溶液中的c(CH3COO-)增大,可以采用升高温度、加入含有醋酸根离子的可能性盐、加入固体碱或加入和氢离子反应的固体物质,使c(H+)减小,可以加碱或加入和氢离子反应的固体物质,故答案为:加NaOH;加Na2CO3等固体;
(5)A.在稀释过程中,溶液的体积增大,氢离子的浓度减小,故A错误;
B.弱电解质越稀,电离度越大,即电离出的氢离子数越多,故B正确;
C.弱电解质越稀,电离度越大,平衡向右移动,CH3COOH分子数减少,故C错误;
D.加水稀释,促进电离,n(CH3COO-)、n(H+)增大,n(CH3COOH)减小,则$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$增大,故D正确;
故答案为:BD.
点评 本题综合考查电解质的电离,侧重于学生的分析能力的考查,为高考常见题型和高频考点,注意加水稀释醋酸,能促进醋酸电离,但溶液中醋酸根离子增大的量远远小于水体积增大的量,所以醋酸根离子浓度减小,为易错点.

| A. | 2 mol/L | B. | 1.5mol/L | C. | 1.0 mol/L | D. | 0.5 mol/L |
| A. | 小苏打-Na2CO3 | B. | 明矾-KAl(SO4)2 | ||
| C. | 漂白粉的有效成分-Ca(ClO)2 | D. | 水玻璃-H2SiO3 |
I.维生素是参与生物生长发育和新陈代谢所必需的一类小分子有机化合物,我们所熟悉的维生素有A、B、C、D、E等.其中
(1)维生素C又称抗坏血酸,人体自身不能合成维生素C;
(2)上述五种维生素中,属于水溶性维生素的是维生素B、维生素C.
Ⅱ.下表是某品牌火腿肠包装上的部分说明.
| 品 名 | ××火腿肠 |
| 部分配料 | ①淀粉 ②味精 ③亚硝酸钠 ④精选瘦肉 |
| 保质期 | 0℃~4℃30天 |
| 生产日期 | 见封口 |
Ⅲ.请将下列食品或药品对应的序号填入相应空格处:
①胃舒平 ②阿司匹林 ③铁强化酱油 ④食用碘盐
(1)预防甲状腺肿大应补充④,
(2)预防贫血应补充③,
(3)感冒患者可服用②,
(4)胃酸过多患者可服用①.
| A. | 5g H2和5g N2 | B. | 224mlN2(标准状况)和0.1molCO | ||
| C. | 16gO2和0.5molSO2 | D. | 22.4LH2O(标准状况)和1molO2 |

