题目内容
【题目】利用钛白工业的副产品FeS04[含A12(S04)3和少量重金属离子]可以生产电池级高纯超微细草酸亚铁。其工艺流程如下:

已知:
①5Fe2++MnO4﹣+8H+═5Fe3++Mn2++4H2O
②5C2O42﹣+2MnO4﹣+16H+═10CO2↑+2Mn2++8H2O
(1)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有_____。
(2)滤液经处理可得到副产品________,可作肥料。
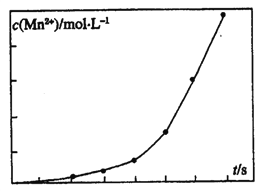
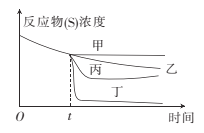
(3)将一定量高锰酸钾溶液与酸化的草酸亚铁溶液混合,测得反应液中Mn2+的浓度随反应时间t的变化如图,其变化趋势的原因可能为_________。
(4)实验室测定高纯超微细草酸亚铁组成的步骤依次为
步骤1:准确称量一定量草酸亚铁样品,加入的H2S04溶解。
步骤2:用0.200 0molL-1标准KMn04溶液滴定,消耗其体积30.40 mL。
步骤3:向滴定后的溶液中加入2gZn粉和5mL2molL-1的H2S04溶液,将Fe3+还原为Fe2+
步骤4:过滤,滤液用上述标准KMn04溶液滴定,消耗溶液10.00 mL.
计算样品中C2O42-的物质的量_________________。(写出计算过程)
【答案】 NH3H2O受热易分解,挥发出NH3,Fe(OH)2受热也易分解 (NH4)2SO4 生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快 0.0102mol
【解析】(1)沉淀过程为一水合氨沉淀亚铁离子的过程,生成氢氧化亚铁,氢氧化亚铁不稳定,受热会分解,另外一水合氨受热也会分解,故反应温度不能太高,所以温度不宜过高的原因除了控制沉淀的粒径外,还有NH3H2O受热易分解,挥发出NH3,Fe(OH)2受热易分解;(2)沉淀前的溶液中含有硫酸亚铁,沉淀步骤中加入一水合氨,生成氢氧化亚铁沉淀和硫酸铵,所以副产品是(NH4)2SO4;(3)从图象上观察,随着反应对进行,曲线的斜率越来越大,说明单位时间内Mn2+的浓度越来越大,所以反应速率越来越快,反应中温度不变,随着反应的进行,反应物的浓度变小,而反应速率加快,只能是生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快;(4)由题意知氧化C2O42-和Fe2+共消耗0.2000 molL-1标准KMnO4溶液体积30.40 mL,步骤3、4标准KMnO4溶液只氧化Fe2+消耗KMnO4溶液体积10.00mL,所以C2O42-消耗KMnO4溶液体积为(30.40-10.00)mL=20.40mL,由5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O得5C2O42-~2MnO4-,所以n(C2O42-)=0.0204L×0.2000molL-1×5/2=0.0102mol。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】将牛奶和姜汁混合,待牛奶凝固便成为一种富有广东特色的甜品——姜撞奶。为了掌握牛奶凝固所需的条件,某同学在不同温度的等量牛奶中混人一些新鲜姜汁,观察混合物15min,看其是否会凝固,结果如下表。请回答下列问题:
温度(℃) | 20 | 40 | 60 | 80 | 100 |
结果 | 15min后仍未有凝固迹象 | 14min内完全凝固 | 1min内完全凝固 | 1min内完全凝固 | 15min后仍未有凝固迹象 |
(注:用曾煮沸的姜汁重复这项实验,牛奶在任何温度下均不能凝固)
(1)实验证明新鲜姜汁中含有一种酶,其作用是 。
(2)20℃和100℃时,15min后仍未有凝固迹象,说明酶的活性较低,其原因分别是 和 。
(3)若60℃时牛奶在有姜汁和没有姜汁的情况下都可以凝固,当反应进行到t时,向其中加人姜汁。下图中能正确表示加姜汁后牛奶凝固随时间变化趋势的曲线是 。
(4)为提高实验的准确度,实验中“不同温度的等量牛奶中混入一些新鲜姜汁”操作中应注意的是 。
(5)有同学说,该实验不能得出姜汁使牛奶凝固的最适温度,请提出解决方案: 。