题目内容
6.已知乙醇的沸点为78.5℃,乙酸的沸点为118℃.今有乙醇和乙酸的无水混合物,某同学拟通过蒸馏的方法分离开.仪器和用品:铁架台(含铁圈)、酒精灯、火柴、石棉网、蒸馏烧瓶、单孔塞、温度计、尾接管、锥形瓶
方案Ⅰ:直接蒸馏
方案Ⅱ:按如下方法蒸馏
实验步骤:
(1)连接好装置、检验装置的气密性.
(2)将混合物加入到蒸馏烧瓶中,并加入适量的试剂a.
(3)加热到97℃,并收集馏分.
(4)冷却后,再向烧瓶中加入试剂b.
(5)加热到118℃,并收集馏分.
请回答问题:
关于方案Ⅰ
(1)如果直接蒸馏会有什么缺点?加热到78.5℃时,大量乙酸也易挥发出来,产品不纯.
关于方案Ⅱ
(2)还缺什么仪器冷凝管;蒸馏属于加热操作,所以操作过程中必须注意实验安全,请你列举两项实验安全措施:加入沸石;规范使用酒精灯.
(3)试剂a最好选用B.
A.苯 B.CaO粉末 C.浓硫酸
加试剂a的作用是让乙酸反应后生成高沸点的离子化合物,以提高乙醇的纯度.
(4)试剂b最好选用A.
A.硫酸 B.硝酸 C.小苏打.
分析 乙醇和乙酸的无水混合物无法用分液的方法分离,就要考虑用蒸馏的方法.但乙醇的沸点为78.5℃,乙酸的沸点为118℃,两者相差不大,所以直接蒸馏有大量乙酸也挥发出来,产品不纯;因此应加碱或碳酸盐等物质,使乙酸生成乙酸盐而拉开两者的沸点.最后向蒸馏出乙醇的母液中加硫酸再蒸馏出乙酸,即可达到分离乙醇和乙酸的目的;
(1)乙酸具有挥发性;
(2)蒸馏装置中要用冷凝管冷凝馏分,蒸馏操作中要加入沸石防止暴沸,要用酒精灯外焰加热;
(3)加入的物质能和乙酸反应生成沸点较高的物质,从而增大与乙醇的沸点差;
(4)加入的物质能和乙酸盐反应生成乙酸,且该物质性质较稳定.
解答 解:乙醇和乙酸的无水混合物无法用分液的方法分离,就要考虑用蒸馏的方法.但乙醇的沸点为78.5℃,乙酸的沸点为118℃,两者相差不大,所以直接蒸馏有大量乙酸也挥发出来,产品不纯.因此应加碱或碳酸盐等物质,使乙酸生成乙酸盐而拉开两者的沸点.最后向蒸馏出乙醇的母液中加硫酸再蒸馏出乙酸,即可达到分离乙醇和乙酸的目的;
(1)乙酸具有挥发性,加热到78.5℃时,大量乙酸也易挥发出来,产品不纯,故答案为:加热到78.5℃时,大量乙酸也易挥发出来,产品不纯;
(2)蒸馏装置中要用冷凝管冷凝馏分,蒸馏操作中要加入沸石防止暴沸,要用酒精灯外焰加热,
故答案为:冷凝管;加入沸石;规范使用酒精灯;
(3)加入的物质能和乙酸反应生成沸点较高的物质,从而增大与乙醇的沸点差,
苯和乙酸不反应,浓硫酸在该混合物中起催化剂作用,使乙酸、乙醇发生酯化反应生成乙酸乙酯,CaO和乙酸反应生成乙酸钙,为离子化合物,熔沸点较高,从而增大与乙醇的沸点差,故选B,
故答案为:B;让乙酸反应后生成高沸点的离子化合物,以提高乙醇的纯度;
(4)加入的物质能和乙酸盐反应生成乙酸,且该物质性质较稳定,
A.硫酸和乙酸钙反应生成乙酸,且稀硫酸没有挥发性,得到的馏分中不含硫酸,故正确;
B.硝酸具有挥发性,得到的馏分中含有硝酸杂质,故错误;
C.小苏打和乙酸钙不反应,所以得不到乙酸,故错误;
故选A.
点评 本题考查物质分离和提纯的综合应用,为高频考点,侧重考查学生实验操作及获取信息利用信息能力,利用物质性质的差异性采取合适的方法进行分离,题目难度不大.

| A. | 油脂有油和脂肪之分,但都属于酯 | |
| B. | 糖类、油脂、蛋白质都能发生水解反应 | |
| C. | 糖类、油脂、蛋白质都是高分子化合物 | |
| D. | 糖类、油脂、蛋白质都是由C、H、O三种元素组成 |
| A. | Cs | B. | O | C. | Be | D. | P |
①测定溶液的pH,溶液显强碱性.
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体.
③在上述②溶液中再滴加Ba(NO3)2溶液,产生白色沉淀.
④取③中上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀.
根据实验以上推测正确的是( )
| A. | 一定有SO32-离子 | B. | 不一定有CO32-离子 | ||
| C. | 不能确定Cl-离子是否存在 | D. | 不能确定HCO3-离子是否存在 |
| A. | 四种元素中,元素Z的非金属性最强 | |
| B. | X、Y、Z三种元素不可能形成离子化合物 | |
| C. | Y、Z、W三种元素的原子半径大小顺序:r(W)>r(Z)>r(Y) | |
| D. | YW3、ZW2、Z2W2中各原子最外层均达到8电子稳定结构 |
| A. | 某离子结构示意图为: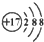 可以表示35Cl-,也可以表示37Cl- 可以表示35Cl-,也可以表示37Cl- | |
| B. | 电子式为: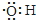 ,可以表示羟基,也可以表示氢氧根离子 ,可以表示羟基,也可以表示氢氧根离子 | |
| C. | 比例模型为: ,可以表示甲烷分子,也可以表示四氯化碳分子 ,可以表示甲烷分子,也可以表示四氯化碳分子 | |
| D. | 晶体锗的结构为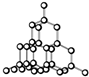 ,其晶胞可表示为 ,其晶胞可表示为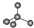 |
| A. | 电子有得失 | B. | 共用电子对有偏移 | ||
| C. | 电子既有得失又有电子对偏移 | D. | 含有多种非金属元素 |
| A. | 无色溶液:Mg2+、NH4+、Cl?、SO42? | |
| B. | 含有0.1mol/L Fe3+的溶液中:Na+、Mg2+、AlO2? | |
| C. | 室温下,pH=3的溶液中:Na+、K+、SiO32?、NO3? | |
| D. | 室温下KW/c(H+)=10?12mol/L的溶液中:Na+、Fe2+、NO3?、SO42? |
