题目内容
下列因果关系成立的是( )
| A、因为NH3的水溶液可以导电,所以NH3是电解质 |
| B、因为Al能与强碱溶液反应,所以Al有一定的非金属性 |
| C、因为某碱性溶液的焰色呈黄色,所以其溶质为NaOH |
| D、因为SO2可以使溴水褪色,所以SO2具有漂白性 |
考点:铝的化学性质,氨的化学性质,二氧化硫的化学性质,钠的重要化合物
专题:元素及其化合物
分析:A.氨气本身不能电离;
B.Al能与强碱溶液反应,与其特性有关;
C.碱性溶液的焰色呈黄色,一定含钠离子;
D.SO2可以使溴水褪色,发生氧化还原反应.
B.Al能与强碱溶液反应,与其特性有关;
C.碱性溶液的焰色呈黄色,一定含钠离子;
D.SO2可以使溴水褪色,发生氧化还原反应.
解答:
解:A.NH3的水溶液可以导电,是因氨气与水反应生成的一水合氨电离出离子,而氨气不能电离,则氨气为非电解质,故A错误;
B.金属一般不能与碱反应,而Al能与强碱溶液反应,体现一定的非金属性,所以Al有一定的非金属性,故B正确;
C.碱性溶液的焰色呈黄色,一定含钠离子,溶液可能为NaOH、纯碱溶液等,故C错误;
D.SO2可以使溴水褪色,发生氧化还原反应,体现二氧化硫的还原性,与漂白性无关,故D错误;
故选B.
B.金属一般不能与碱反应,而Al能与强碱溶液反应,体现一定的非金属性,所以Al有一定的非金属性,故B正确;
C.碱性溶液的焰色呈黄色,一定含钠离子,溶液可能为NaOH、纯碱溶液等,故C错误;
D.SO2可以使溴水褪色,发生氧化还原反应,体现二氧化硫的还原性,与漂白性无关,故D错误;
故选B.
点评:本题考查物质的性质,为高频考点,综合考查元素化合物知识,把握物质的性质及发生的反应、焰色反应、电解质的判断等为解答的关键,侧重分析与知识综合应用能力的考查,题目难度不大.

练习册系列答案
相关题目
下列各组离子,在pH=0的溶液中可以大量共存的是( )
| A、Al3+、Fe3+、Br-、SO42- |
| B、K+、Ca2+、SO42-、Cl- |
| C、Na+、Cu2+、I-、NO3- |
| D、NH4+、K+、HPO42-、Cl- |
下列关于硅的说法不正确的是( )
| A、硅是非金属元素,它的单质是灰黑色有金属光泽的固体 |
| B、硅的导电性能介于金属和绝缘体之间,是良好的半导体材料 |
| C、加热到一定温度时,硅能与氢气、氧气等非金属反应 |
| D、硅的化学性质不活泼,常温下不与任何物质起反应 |
下列事实不能说明一元酸HA为弱酸的是( )
| A、常温下0.1mol?L-1的HA溶液pH为5 |
| B、常温下NaA溶液的pH>7 |
| C、HA溶液中存在H+、OH-、A-、HA |
| D、HA溶液能与大理石反应 |
下列说法正确的是( )
| A、反应:2CO(g)+2NO(g)?N2(g)+2CO2(g)在温度为298K时能自发进行,则它的△H>0,△S>0 |
| B、镀锌铁破损后会加快铁的腐蚀 |
| C、为保护浸入海水中的钢闸门,可在闸门表面镶上铜锭 |
| D、反应:2A(g)?B(g)+2C(g),增大压强反应速率加快,A的转化率减小 |
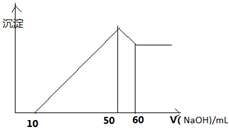 某溶液中含有H+、Al3+、Mg2+、Cu2+四种阳离子,且Mg2+ Cu2+物质的量之为1:1,逐滴加入0.1moL/L NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如图所示,则溶液中H+、Al3+、Mg2+、Cu2+四种阳离子的物质的量浓度之比为( )
某溶液中含有H+、Al3+、Mg2+、Cu2+四种阳离子,且Mg2+ Cu2+物质的量之为1:1,逐滴加入0.1moL/L NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如图所示,则溶液中H+、Al3+、Mg2+、Cu2+四种阳离子的物质的量浓度之比为( )| A、1:1:1:1 |
| B、2:2:1:1 |
| C、2:1:1:1 |
| D、4:4:1:1 |
下列关于钠说法中错误的是( )
| A、金属钠在空气中燃烧,生成氧化钠 |
| B、钠是密度比水小的金属单质,能浮在水面上 |
| C、钠是银白色、质软、熔点相对较低 |
| D、将金属钠放在石棉网上用酒精灯加热后,金属钠剧烈燃烧,产生黄色火焰. |
以下化学反应属于复分解反应的是( )
| A、CaO+H20═Ca(OH)2 | ||||
B、Fe2O3+3CO
| ||||
| C、Cl2+2KBr═2KCl+Br2 | ||||
| D、Na2CO3+BaCl2═2NaCl+BaCO3↓ |
下列有关热化学方程式的叙述正确的是( )
| A、在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,若将含0.6mol H2SO4的稀硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3kJ |
| B、已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C、需要加热的反应说明它是吸热反应 |
| D、已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |