题目内容
【题目】磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。一种回收废旧磷酸亚铁锂电池正极片(主要成分LiFePO4、炭黑和铝箔)中金属的流程如下:
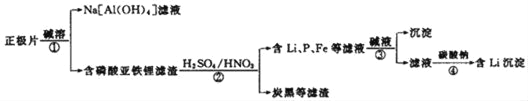
(1)步骤①中“碱溶”反应的化学方程式为_____。
(2)步骤②中反应的离子方程式为_____。若用H2O2代替HNO3,其优点是_____。
(3)步骤③沉淀的主要成分是_____。
(4)步骤④中生成含Li沉淀_____(填“能”或“不能”)用硫酸钠代替碳酸钠,原因是_____。
【答案】2Al+2NaOH+6H2O=3H2↑+2Na[Al(OH)4] 3LiFePO4+NO3﹣+13H+=3Li++3Fe3++3H3PO4+NO↑+2H2O 不产生氮氧化物大气污染物 Fe(OH)3 不能 硫酸锂易溶于水,不能形成含锂沉淀 。
【解析】
步骤①中“碱溶”反应的化学方程式为2Al+2NaOH+6H2O=3H2↑+2Na[Al(OH)4],过滤分离出铝元素,步骤②滤渣中加入氧化性酸硝酸,将亚铁离子氧化为铁离子,强酸制弱酸有磷酸生成,产物为Li+、Fe3+、H3PO4、NO,加入碱液,铁离子生成Fe(OH)3沉淀,过滤分离出铁元素,滤液中加入碳酸钠,生成碳酸锂沉淀。
(1)步骤①中“碱溶”反应的化学方程式为2Al+2NaOH+6H2O=3H2↑+2Na[Al(OH)4];
答案:2Al+2NaOH+6H2O=3H2↑+2Na[Al(OH)4]。
(2)步骤②中反应的离子方程式为3LiFePO4+NO3﹣+13H+=3Li++3Fe3++3H3PO4+NO↑+2H2O,若用H2O2代替HNO3,其优点是不产生氮氧化物大气污染物;
答案:3LiFePO4+NO3﹣+13H+=3Li++3Fe3++3H3PO4+NO↑+2H2O;不产生氮氧化物大气污染物。
(3)由以上分析可知步骤③沉淀的主要成分是Fe(OH)3;
答案:Fe(OH)3。
(4)硫酸锂易溶于水,不能用硫酸钠代替碳酸钠;
答案:不能;硫酸锂易溶于水,不能形成含锂沉淀。