题目内容
【题目】现有14.4 gCO和CO2的混合气体,在标准状况下,其体积为8.96L。回答下列问题:
(1)该混合气体的平均摩尔质量为__________。
(2)混合气体中碳原子的个数为________(用NA表示阿伏加德罗常数的值)。
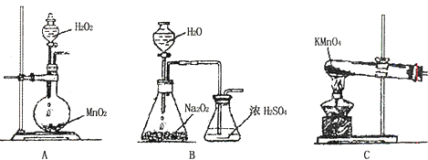
(3)将混合气体依次通过如下图所示装置,剩余气体最后收集在气球中(实验在标准状况下测定)。
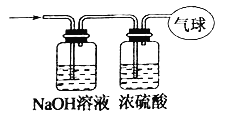
气球中收集到的气体的摩尔质量为__________。
气球中收集到的气体中,电子总数为____________(用NA表示阿伏加德罗常数的值)。
气球的体积为____________L。
【答案】
(1)36g/mol
(2)0.4 NA
(3)①28 g/mol;② 2.8 NA;③4.48
【解析】
试题分析:(1)混合气体的体积为8.96L,则物质的量为其物质的量为:n=![]() =
=![]() =0.4mol,混合气体的平均摩尔质量为:
=0.4mol,混合气体的平均摩尔质量为:![]() =36g/mol,故答案为:36g/mol;
=36g/mol,故答案为:36g/mol;
(2)设混合气体中CO的物质的量为xmol,CO2的物质的量为ymol,则根据混合物的质量为14.4g可得:28x+44y=14.4 ①;根据气体的物质的量为0.4mol可得:x+y=0.4 ②,解①②得:x=0.2mol、y=0.2mol,由于CO和CO2中均含1个碳原子,故0.2molCO和0.2molCO2中共含0.4molC原子即0.4NA个,故答案为:0.4NA;
(3)将混合气体依次通过如图装置,则CO2会被NaOH溶液吸收,剩余CO,被浓硫酸干燥后,则在气球中收集到的是干燥纯净的CO气体.
①气球中收集到的气体为CO,而一种物质的摩尔质量在数值上等于该物质的相对分子质量,故收集到气体的摩尔质量为28g/mol,故答案为:28g/mol;
②一个CO含有14个电子,由(2)求出的CO的物质的量为0.2mol,则电子的物质的量为0.2mol×14=2.8mol,电子总数为2.8NA个;故答案为:2.8NA;
③气球中的气体为CO,其体积V=nVm=0.2mol×22.4L/mol=4.48L,故答案为:4.48。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案