题目内容
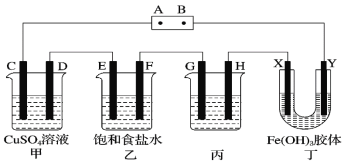
【题目】某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:
(1)电源A极的名称是________。
(2)甲装置中电解反应的总化学方程式为(电解质溶液是足量的):_______电解后若使电解质溶液复原需要加入适量的__________________
(3)如果收集乙装置中产生的气体,两种气体的体积比是(忽略气体的溶解)________。ClO2为一种黄绿色气体,是目前国际上公认的高效、广谱、快速安全的杀菌剂。制备ClO2的新工艺是电解法。若调控合适的电压可以利用乙装置制备ClO2,写出阳极产生ClO2的电极反应式__________ClO2对污水中Fe2+、Mn2+、S2-、CN-等有明显去除效果,某工厂污水中含CN-,现用ClO2把CN-氧化成两种无毒气体,写出该反应的离子方程式:_____________。
(4)欲用丙装置给铜镀银,G应该是________(填“铜”或“银”),电镀液的主要成分是________(填化学式)。
(5)装置丁中的现象是_______。
【答案】正极 2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4 CuO 1∶1 Cl--5e-+2H2O===ClO2↑+4H+ 2ClO2+2CN-===N2+2CO2+2Cl- 银 AgNO3 Y极附近红褐色变深
2Cu+O2↑+2H2SO4 CuO 1∶1 Cl--5e-+2H2O===ClO2↑+4H+ 2ClO2+2CN-===N2+2CO2+2Cl- 银 AgNO3 Y极附近红褐色变深
【解析】
将电源接通后,向乙中滴入酚酞试液,在F极附近显红色,说明F极生成OH-,F为阴极,则可以知道A为正极,B为负极,C、E、G、X为阳极,D、F、H、Y为阴极;电解饱和食盐水时,酚酞变红的极是阴极,阴极和电源负极相连;电解硫酸铜溶液生成硫酸、铜和氧气;电解饱和食盐水生成氢氧化钠、氯气和氢气;铜上镀银,金属银做阳极,电镀液为硝酸银;氢氧化铁胶体中含有的带正电荷的粒子,在电场的作用下会向阴极移动,据此分析体系颜色的变化;结合以上分析进行解答。
将电源接通后,向乙中滴入酚酞试液,在F极附近显红色,说明F极生成OH-,F为阴极,则可以知道A为正极,B为负极,C、E、G、X为阳极,D、F、H、Y为阴极,
(1)由以上分析可以知道A是电源的正极,B是原电池的负极;
答案是:正极;
(2)惰性电极电解硫酸铜溶液生成硫酸、铜和氧气,电解方程式为:2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4;反应后生成了铜和氧气,因此电解后若使电解质溶液复原需要加入适量的CuO;
2Cu+O2↑+2H2SO4;反应后生成了铜和氧气,因此电解后若使电解质溶液复原需要加入适量的CuO;
答案是:2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4;CuO;
2Cu+O2↑+2H2SO4;CuO;
(3)乙装置为电解饱和食盐水,总反应为:2NaCl+2H2O![]() 2NaOH+Cl2↑+ H2↑;据此可知两种气体的体积比是1:1;根据题意可以知道,氯离子放电生成ClO2,由元素守恒可以知道,有水参加反应,同时生成氢离子,电极反应式为: Cl--5e-+2H2O===ClO2↑+4H+;ClO2把CN-氧化成N2和CO2两种无毒气体,反应的离子方程式为:2ClO2+2CN-===N2+2CO2+2Cl-;
2NaOH+Cl2↑+ H2↑;据此可知两种气体的体积比是1:1;根据题意可以知道,氯离子放电生成ClO2,由元素守恒可以知道,有水参加反应,同时生成氢离子,电极反应式为: Cl--5e-+2H2O===ClO2↑+4H+;ClO2把CN-氧化成N2和CO2两种无毒气体,反应的离子方程式为:2ClO2+2CN-===N2+2CO2+2Cl-;
故答案是:1∶1;Cl--5e-+2H2O===ClO2↑+4H+ ;2ClO2+2CN-===N2+2CO2+2Cl- ;
(4) 欲用丙装置给铜镀银,金属铜应连在电源的负极上,做电解池的阴极,银与电源的正极相连,做电解池的阳极,电镀液的主要成分是硝酸银;
故答案是:银;AgNO3;
(5) 根据异性电荷相吸的原理,氢氧化铁胶体中含有的带正电荷的粒子会向阴极即Y极移动,所以Y极附近红褐色变深;
答案是:Y极附近红褐色变深。