题目内容
【题目】常温下,用0.1 mol/LNaOH溶液滴定10mL 0.1mol/LH2A溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列说法不正确的是( )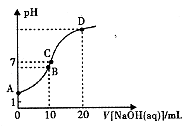
A.A点溶液中加入少量水: ![]() 增大
增大
B.B点:c( HA ﹣)>c(H+)>c(A2-)>c(H2A)
C.C点:c(Na+)=c(HA﹣)+2c( A2﹣)
D.水电离出来的c(OH﹣):B点>D点
【答案】D
【解析】解:A.根据图象可知,0.1mol/L的H2A溶液的pH大于1,说明H2A为弱酸,若A点溶液中加入少量水,溶液中氢离子、H2A的浓度减小,由于水的离子积不变,则氢氧根离子浓度增大,所以 ![]() 的比值增大,故A正确;
的比值增大,故A正确;
B.B点时加入了10mLNaOH溶液,反应后溶质为NaHA,此时溶液的pH小于7,说明HA﹣的电离程度大于其水解程度,则c(A2﹣)>c(H2A),由于氢离子还来自水的电离,则c(H+)>c(A2﹣),溶液中离子浓度大小为:c( HA ﹣)>c(H+)>c(A2﹣)>c(H2A),故B正确;
C.C点溶液的pH=7,为中性溶液,则c(H+)=c(OH﹣),根据电荷守恒c(Na+)+c(H+)=c(HA﹣)+2c( A2﹣)+c(OH﹣)可知:c(Na+)=c(HA﹣)+2c( A2﹣),故C正确;
D.B点反应后溶质为NaHA,HA﹣的电离程度大于其水解程度,溶液呈酸性,氢离子抑制了水的电离,而D点加入20mL氢氧化钠溶液,二者恰好反应生成Na2A,A2﹣水解促进了水的电离,所以水电离的c(OH﹣):B点<D点,故D错误;
故选D.

练习册系列答案
相关题目