题目内容
【题目】孔雀石的主要成分是![]() ,还含有少量
,还含有少量![]() 、
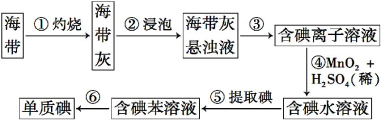
、![]() 等杂质,实验室以孔雀石为原料制备硫酸铜晶体流程如下:
等杂质,实验室以孔雀石为原料制备硫酸铜晶体流程如下:

已知相关氢氧化物沉淀的pH范围如下:
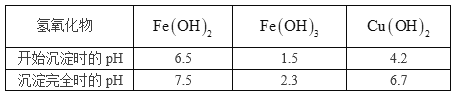
完成下列填空:
(1)滤液1中含有的金属阳离子有_______________。
(2)步骤②中所用的试剂X是________(选填编号)。
a. Fe粉 b. ![]() c. 氨水 d. KSCN
c. 氨水 d. KSCN
(3)步骤③中加入CuO的目的是________________________________________。
(4)由滤液3得到硫酸铜晶体,需要经过的步骤依次有:_________、________、过滤等。
(5)为测定所得晶体中结晶水的![]() 值,可采用加热法。取
值,可采用加热法。取![]() g晶体灼烧至结晶水全部失去,称得无水硫酸铜的质量bg。
g晶体灼烧至结晶水全部失去,称得无水硫酸铜的质量bg。
①晶体应盛装在________(填仪器名称)中进行灼烧。
②确认结晶水已全部失去的方法是___________________________。
③![]() 值的表达式为______________(用
值的表达式为______________(用![]() 、
、![]() 表示)。
表示)。
④实验结果发现测得结晶水数量![]() 偏高,可能的原因有___________(任写一种)。
偏高,可能的原因有___________(任写一种)。
【答案】 Cu2+、Fe2+ b 调节溶液的pH,使Fe3+沉淀的同时不引入新的杂质 蒸发浓缩 降温结晶 坩埚 前后两次称量无水硫酸铜的质量差小于0.001g 80(a-b)/9b 加热前称量时坩埚未完全干燥、加热过程中有少量晶体溅出、加热时坩埚内质量变黑等,合理即可
【解析】试题分析:由流程可知,孔雀石经稀硫酸溶解后,其中的碱式碳酸铜和碳酸亚铁皆可溶解,过滤得到硫酸铜和硫酸亚铁溶液,向滤液中加入氧化剂X把亚铁离子氧化,再加入CuO调节溶液的pH,除去溶液中的铁离子,过滤,将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥即可得到产品。
(1)滤液1中含有的金属阳离子有Cu2+、Fe2+。
(2)步骤②中所用的试剂X是氧化剂,以双氧水为最佳,其他几个不能把亚铁离子氧化,故选b。
(3)步骤③中加入CuO的目的是调节溶液的pH,使Fe3+沉淀的同时不引入新的杂质。
(4)由滤液3得到硫酸铜晶体,需要经过的步骤依次有:蒸发浓缩、降温结晶、过滤等。
(5)为测定所得晶体中结晶水的![]() 值,可采用加热法。取
值,可采用加热法。取![]() g晶体的烧至结晶水全部失去,称得无水硫酸铜的质量bg。
g晶体的烧至结晶水全部失去,称得无水硫酸铜的质量bg。
①通常在坩埚中灼烧固体,故晶体应盛装在坩埚中进行灼烧。
②确认结晶水已全部失去的方法是前后两次称量无水硫酸铜的质量差小于0.001g。
③![]() g晶体的烧至结晶水全部失去,称得无水硫酸铜的质量bg,则结晶水的质量为(a-b)g,结晶水的物质的量为
g晶体的烧至结晶水全部失去,称得无水硫酸铜的质量bg,则结晶水的质量为(a-b)g,结晶水的物质的量为![]() ,bg硫酸铜的物质的量为
,bg硫酸铜的物质的量为![]() ,所以,
,所以, ![]() 值的表达式为80(a-b)/9b。
值的表达式为80(a-b)/9b。
④实验结果发现测得结晶水数量![]() 偏高,可能的原因有:加热前称量时坩埚未完全干燥、加热过程中有少量晶体溅出、加热时坩埚内质量变黑(硫酸铜部分分解生成黑色的氧化铜)等。
偏高,可能的原因有:加热前称量时坩埚未完全干燥、加热过程中有少量晶体溅出、加热时坩埚内质量变黑(硫酸铜部分分解生成黑色的氧化铜)等。

 名校课堂系列答案
名校课堂系列答案