题目内容
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。
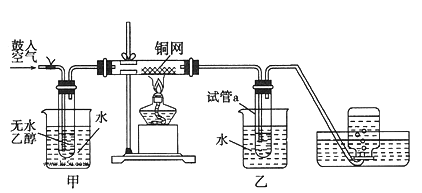
(1)实验过程中铜网出现黑色和红色交替的现象,请写出相应的化学方程式:
________________________,_____________________________ 。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是_____反应。
(2)甲和乙两个水浴作用不相同。甲的作用是___________;乙的作用是____________。
(3)反应进行一段时间后,试管a中能收集到不同的物质,它们是____________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有_____(填写名称)。
【答案】 2Cu+O2![]() 2CuO CH3CH2OH+CuO
2CuO CH3CH2OH+CuO![]() CH3CHO+Cu+H2O 放热 加热 冷却 乙醛、乙醇、水(至少答对两种) 乙酸
CH3CHO+Cu+H2O 放热 加热 冷却 乙醛、乙醇、水(至少答对两种) 乙酸
【解析】(1)铜丝变黑是因为发生反应:2Cu+O2![]() 2CuO;后来变红是因为发生反应:CH3CH2OH+CuO
2CuO;后来变红是因为发生反应:CH3CH2OH+CuO![]() CH3CHO+Cu+H2O;熄灭酒精灯,反应仍能继续进行,说明该反应是放热反应。
CH3CHO+Cu+H2O;熄灭酒精灯,反应仍能继续进行,说明该反应是放热反应。
(2)根据反应流程可知:在甲处用热水浴加热,使乙醇挥发与空气中的氧气混合,有利于下一步催化氧化反应的顺利进行;乙处用冷水浴冷却,降低温度,使生成的乙醛冷凝成为液体,沉在试管的底部。
(3)反应进行一段时间后,试管a中能收集到不同的物质,它们是:未反应的乙醇、生成的乙醛和水。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有酸性物质,根据碳原子守恒推测生成了乙酸,乙醛氧化生成了乙酸。

 一线名师权威作业本系列答案
一线名师权威作业本系列答案【题目】某同学在研究元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
实验步骤 | 实验现象 |
①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色 |
②向新制的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
④将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
⑥向AlCl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究__________________元素性质递变规律。
(2)实验用品:试剂:金属钠、镁条、铝条、稀盐酸、新制氯水、新制Na2S溶液、AlCl3溶液、NaOH溶液、酚酞溶液等。
仪器:______、______、滤纸、试管夹、胶头滴管、镊子、小刀、玻璃片、砂纸、火柴等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式及此实验的结论)
实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
实验现象(填A~F) | __ | __ | __ | __ | __ | __ |
①__________________________________________________;
②___________________________________________________;
此实验的结论:__________________________________________________。