题目内容
【题目】研究证明高铁酸钠(Na2FeO4) 是一种“绿色环保高效”消毒剂, 比目前国内外广泛使用的含氯饮用水消毒剂性能更为优良。高铁酸钠只能在碱性环境中稳定存在。下列是通过次氯酸钠氧化法制备高铁酸钠并探究其性质的实验,步骤如下:
I.用氯气和氢氧化钠溶液反应制备NaClO溶液

(1)A是氯气发生装置,写出实验室用此装置制取氯气的离子方程式__________。
(2)I装置的作用是__________ 。
(3)用图示的II或III代替I是否可行? __________。简要说明理由__________ 。
(4)将产生的氯气通入D装置中制NaClO溶液
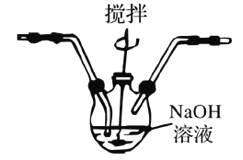
已知:3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O 为了防止产生NaClO3,除搅拌和混入N2稀释外,还应采取的操作是__________。
5NaCl+NaClO3+3H2O 为了防止产生NaClO3,除搅拌和混入N2稀释外,还应采取的操作是__________。
II.制备Na2FeO4
(1)将Fe(NO3)3溶液加入到NaOH与NaClO的混合溶液中,其反应的离子方程式是______。过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品,上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是__________。
(2)高铁酸钠电池是一种新型可充电电池,电解质为NaOH溶液,放电时负极材料为Zn,正极产生红褐色沉淀,写出该电池反应的化学方程式__________。
【答案】 MnO2+4H++2C1- ![]() Mn2++Cl2↑+2H2O 收集并储存氯气 Ⅱ可行,Ⅲ不行 Ⅱ与Ⅰ原理相同,而Ⅲ中因c瓶口密封,体积不能改变,增大压强会有危险,且由于B、C液差太小,不能使储存的Cl2全部排出 将D放在冷水中 2Fe3++ 3C1O-+ 10OH-==2FeO42-+ 3Cl-+5H2O Na2FeO4在水溶液中水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失 3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH
Mn2++Cl2↑+2H2O 收集并储存氯气 Ⅱ可行,Ⅲ不行 Ⅱ与Ⅰ原理相同,而Ⅲ中因c瓶口密封,体积不能改变,增大压强会有危险,且由于B、C液差太小,不能使储存的Cl2全部排出 将D放在冷水中 2Fe3++ 3C1O-+ 10OH-==2FeO42-+ 3Cl-+5H2O Na2FeO4在水溶液中水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失 3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH
【解析】I. (1)①实验室用二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水,离子方程式为:MnO2+4H++2C1- ![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
②从装置图可看出,I装置的作用是收集并储存氯气;
(3)比较装置Ⅰ、Ⅱ和Ⅲ发现,Ⅱ与Ⅰ原理相同,而Ⅲ中因c瓶口密封,体积不能改变,增大压强会有危险,且由于B、C液差太小,不能使储存的Cl2全部排出。
(4) 温度过高会发生反应:3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O,所以为了防止产生NaClO3应将D放在冷水中。
5NaCl+NaClO3+3H2O,所以为了防止产生NaClO3应将D放在冷水中。
II. (1)Fe3+与在碱性条件下被ClO-氧化生成FeO42-本身被还原为Cl-,其反应的离子方程式是2Fe3++ 3C1O-+ 10OH-==2FeO42-+ 3Cl-+5H2O;由于Na2FeO4在水溶液中水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失,所以要用NaOH溶液溶解粗产品而不用水。因此,本题答案为:2Fe3++ 3C1O-+ 10OH-==2FeO42-+ 3Cl-+5H2O ;Na2FeO4在水溶液中水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失。
(2)负极是锌,失去电子在氢氧化钠的条件下生成氢氧化锌,高铁酸钠转化为氢氧化铁红褐色沉淀,电池反应为: 3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH,因此,本题正确答案是: 3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH。