题目内容
将一定量的CO2气体通入500 mL某NaOH溶液中,充分反应后,将溶液在低温下蒸发,得到不含结晶水的白色固体A。取三份质量不同的A样品分别与50 mL相同浓度的盐酸反应,得到的气体在标准状况下的体积与固体A的质量关系如下表所示:组别 | 1 | 2 | 3 |
盐酸体积/Ml | 50 | 50 | 50 |
A的质量/g | 3.8 | 6.2 | 7.2 |
气体体积/L | 0.90 | 1.3 | 1.3 |
(1)从表中第_________________________组数据表明加入的50 mL盐酸反应后剩余,理由是_____________________________________。
(2)试求A是什么物质,其成分的质量分数各是多少?
(1)1 第一组中A的质量为
(2)A是Na2CO3和NaHCO3的混合物;
w (Na2CO3)=56%,w(NaHCO3)=44%。
解析:分析表中结果可知,同样是50 mL盐酸,第1组中A的质量为
因为在第1组中,n(CO2)=![]() =0.04 mol。
=0.04 mol。
若A为Na2CO3,则m(Na2CO3)=0.04 mol×
若A为NaHCO3,则m(NaHCO3)=0.04 mol×
故A为Na2CO3和NaHCO3的混合物。
设第1组中Na2CO3的物质的量为x,NaHCO3的物质的量为y,则
![]()
![]()

将一定量的CO2气体通入500mL某NaOH溶液中,充分反应后,将溶液在低温进行蒸发,得到不含结晶水的白色固体A。取三份质量不同的A样品分别与50mL相同浓度的盐酸反应,得到气体的体积(标准状况)与固体A的质量关系如下表所示:
|
组 别 |
1 |
2 |
3 |
|
盐酸体积(mL) |
50 |
50 |
50 |
|
A的质量(g) |
3.80 |
5.70 |
7.60 |
|
气体体积(mL) |
896 |
1344 |
1344 |
(1)上表中第 组数据加入的50mL盐酸的反应后有剩余,
(2)试推断:A的成份为
(3)盐酸的物质的量的浓度为 mol·L-1
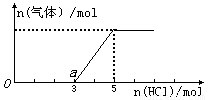
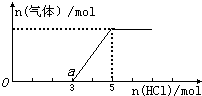 将一定量的CO2气体通入2L的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量关系如图所示(忽略气体的溶解和HCl的挥发).
将一定量的CO2气体通入2L的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量关系如图所示(忽略气体的溶解和HCl的挥发).