题目内容
5.NA代表阿伏加德罗常数,下列说法正确的是( )| A. | 2.4 g金属镁在反应中全部变成镁离子时,失去的电子数目为0.1NA | |
| B. | 2 g氢气所含氢原子数目为NA | |
| C. | 17 g OH- 所含的质子数目为10NA | |
| D. | 58.5 g NaCl中所含有的Na+离子数目为NA |
分析 A、根据镁的质量计算出物质的量,再根据电子守恒进行计算失去电子数;
B、氢气分子是双原子分子;
C、求出OH-的物质的量,然后根据1molOH-中含9mol质子来分析;
D、求出氯化钠的物质的量,然后根据1mol氯化钠中含1mol钠离子来分析.
解答 解:A、2.4g镁的物质的量为0.1mol,完全反应生成镁离子失去0.2mol电子,失去的电子数目为0.2NA,故A错误;
B、氢气分子是双原子分子,2g氢气所含氢原子数目为2NA,故B错误;
C、17gOH-的物质的量n=$\frac{17g}{17g/mol}$=1mol,而1molOH-中含9mol质子即9NA个,故C错误;
D、58.5g氯化钠的物质的量n=$\frac{58.5g}{58.5g/mol}$=1mol,而1mol氯化钠中含1mol钠离子,即NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
20.下列实验操作正确的是( )
| A. | Na2S2O3与硫酸反应的实验中,实验室没有硫酸,临时用硝酸进行实验 | |
| B. | 滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定 | |
| C. | 制取氯气时,用二氧化锰与浓盐酸在加热下反应,并用排水集气法收集 | |
| D. | 配制FeCl3溶液时,将FeCl3溶解在较浓的盐酸中,用水稀释到所需浓度 |
10.在下列溶液中,一定能够大量共存的离子组是( )
| A. | 常温下,由水电离出的c(H+)=l0-14mo1•L-1的溶液中:CO32-、SO42-、Na+、K+ | |
| B. | 滴加石蕊试液显红色的溶液:Fe3+、NH4+、C1-、CN- | |
| C. | pH为1的溶液:Ca2+、Na+、Mg2+、NO3- | |
| D. | 与铝反应放出氢气的溶液:Fe2+、SO42-、NO3-、Na+ |
17.下列有关化学用语表示正确的是( )
| A. | 四氯化碳分子的比例模型 | B. | 次氯酸的结构式为H-Cl-O | ||
| C. | CO2的电子式是: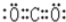 | D. | ${\;}_{8}^{18}$O2-离子结构示意图: |
14.为了探究Cu(NO3)2的氧化性和热稳定性,某化学兴趣小组设计了如下实验.
Ⅰ.Cu(NO3)2 的氧化性
将光亮的铁丝伸入Cu(NO3)2 溶液中,一段时间后将铁丝取出.为检验溶液中Fe 的氧化产物,将
溶液中的Cu2+除尽后,进行了如下实验.可选用的试剂KSCN 溶液、K3[Fe(CN)6]溶液、氯水.
(1)请完成下表:
Ⅱ.Cu(NO3)2的热稳定性
在如图1所示的实验装置A 中,用酒精喷灯对Cu(NO3)2 固体加强热,产生红棕色气体,在装置C中收集到无色气体,经验证为O2.当反应结束以后,试管中残留固体为红色.

(2)装置B 的作用是除去混合气体中的NO2.
(3)从实验安全角度考虑,需要在A、B 间加入装置M,请在方框中如图2出M 装置
(4)如图3为Cu(NO3)2 样品高温过程的热重曲线(样品质量分数w%随温度变化的曲线).Cu(NO3)2
加热到200℃的化学方程式为2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$ 2CuO+4NO2↑+O2↑,继续高温至1000℃生成Cu2O(填化学式)固体.
Ⅰ.Cu(NO3)2 的氧化性
将光亮的铁丝伸入Cu(NO3)2 溶液中,一段时间后将铁丝取出.为检验溶液中Fe 的氧化产物,将
溶液中的Cu2+除尽后,进行了如下实验.可选用的试剂KSCN 溶液、K3[Fe(CN)6]溶液、氯水.
(1)请完成下表:
| 操作 | 反应或现象 | 结论 |
| 取少量除尽Cu2+后的溶液于试管中,加入①溶液,振荡 | 显性② | 存在Fe3+ |
| 取少量除尽Cu2+后的溶液于试管中,加入K3[Fe(CN)6]溶液,振荡 | 离子方程式③ | 存在Fe2+ |
在如图1所示的实验装置A 中,用酒精喷灯对Cu(NO3)2 固体加强热,产生红棕色气体,在装置C中收集到无色气体,经验证为O2.当反应结束以后,试管中残留固体为红色.

(2)装置B 的作用是除去混合气体中的NO2.
(3)从实验安全角度考虑,需要在A、B 间加入装置M,请在方框中如图2出M 装置
(4)如图3为Cu(NO3)2 样品高温过程的热重曲线(样品质量分数w%随温度变化的曲线).Cu(NO3)2
加热到200℃的化学方程式为2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$ 2CuO+4NO2↑+O2↑,继续高温至1000℃生成Cu2O(填化学式)固体.
15.下列有关物质的使用叙述不合理的是( )
| A. | 亚硝酸钠是常用的防腐剂 | |
| B. | 婴儿食品可添加着色剂,以增加婴儿对食物的兴趣 | |
| C. | 食用盐既可以做防腐剂,又可以做调味剂 | |
| D. | 药物可以帮助我们战胜疾病,但我们仍需合理用药 |