��Ŀ����
14��Ϊ��̽��Cu��NO3��2�������Ժ����ȶ��ԣ�ij��ѧ��ȤС�����������ʵ�飮��Cu��NO3��2 ��������
����������˿����Cu��NO3��2 ��Һ�У�һ��ʱ�����˿ȡ����Ϊ������Һ��Fe �����������
��Һ�е�Cu2+��������������ʵ�飮��ѡ�õ��Լ�KSCN ��Һ��K3[Fe��CN��6]��Һ����ˮ��
��1��������±���
| ���� | ��Ӧ������ | ���� |
| ȡ��������Cu2+�����Һ���Թ��У��������Һ���� | ���Ԣ� | ����Fe3+ |
| ȡ��������Cu2+�����Һ���Թ��У�����K3[Fe��CN��6]��Һ���� | ���ӷ���ʽ�� | ����Fe2+ |
����ͼ1��ʾ��ʵ��װ��A �У��þƾ���ƶ�Cu��NO3��2 �����ǿ�ȣ���������ɫ���壬��װ��C���ռ�����ɫ���壬����֤ΪO2������Ӧ�����Ժ��Թ��в�������Ϊ��ɫ��

��2��װ��B �������dz�ȥ��������е�NO2��
��3����ʵ�鰲ȫ�Ƕȿ��ǣ���Ҫ��A��B �����װ��M�����ڷ�������ͼ2��M װ��
��4����ͼ3ΪCu��NO3��2 ��Ʒ���¹��̵��������ߣ���Ʒ��������w%���¶ȱ仯�����ߣ���Cu��NO3��2
���ȵ�200��Ļ�ѧ����ʽΪ2Cu��NO3��2$\frac{\underline{\;\;��\;\;}}{\;}$ 2CuO+4NO2��+O2��������������1000������Cu2O���ѧʽ�����壮
���� ��1�������������������Һ��Ӧ����Ѫ��ɫ��Һ��֤�����ӵĴ��ڣ��������ӵļ�����K3[Fe��CN��6]��Һ���������ӽ��������ɫ�������ݴ˽��н��
��2����������װ��A���þƾ����ǿ�ȣ���������ɫ����Ϊ������������װ��C���ռ�����ɫ���壬��֪װ��B�ж�������������������Һ������Ӧ��
��3��Ϊ�˷�ֹCװ���е�Һ�嵽���뷢��װ��A����Ҫ��A��B ����밲ȫƿ���л������ã�
��4������M��Cu��NO3��2����w%=��������Ħ�������������Ħ��������Ȼ���������ʽ����ʵ���֪���в������������������Ȼ����д����ʽ��
��� �⣺��1��ȡ��������Cu2+�����Һ���Թ��У�����KSCN��Һ������������������Һ���Ѫ��ɫ����֤����ȡ��������Cu2+�����Һ���Թ��У�����K3[Fe��CN��6]��Һ��K3[Fe��CN��6]���������ӷ�Ӧ������ɫ������
����ʽΪ��2[Fe��CN��6]3-+3Fe2+�TFe3[Fe��CN��6]2����
�ʴ�Ϊ����KSCN��Һ������Һ�ʺ�ɫ����2[Fe��CN��6]3-+3Fe2+�TFe3[Fe��CN��6]2����
��2��װ��B�������dz�ȥ��������е�NO2��
�ʴ�Ϊ����ȥ��������е�NO2��
��3����ȫƿ�е�������¶����������ͼ��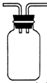 �����Է�ֹCװ���е�Һ�嵽���뷢��װ��A��
�����Է�ֹCװ���е�Һ�嵽���뷢��װ��A��
�ʴ�Ϊ�� ��
��
��4��Cu��NO3��2���ȵ�200��ʱ��M��Cu��NO3��2����w%=188g/mol��42.6%=80g/mol��ǡ����CuO��Ħ����������ʵ���֪���в����������������������ʽΪ��2Cu��NO3��2$\frac{\underline{\;\;��\;\;}}{\;}$ 2CuO+4NO2��+O2��������������1000��ʱ��M��Cu��NO3��2����w%=188g/mol��38.3%=72g/mol��ǡ���ǹ���Cu2O��Ħ��������һ�룬�ʲ���Ϊ����Cu2O��
�ʴ�Ϊ��2Cu��NO3��2$\frac{\underline{\;\;��\;\;}}{\;}$ 2CuO+4NO2��+O2����Cu2O��
���� ���⿼�����������ʵ�̽�����漰ͼ��������㣬ʵ��ԭ����ע��ʵ����̷����жϣ������������ʺ����ݷ����ǽ���ؼ�����Ŀ�ѶȽϴ�

| A�� | ����+Na2CO3 | B�� | ����+NaOH | C�� | ����+�Ҵ� | D�� | ����+Fe |
| A�� | 2.4 g����þ�ڷ�Ӧ��ȫ�����þ����ʱ��ʧȥ�ĵ�����ĿΪ0.1NA | |
| B�� | 2 g����������ԭ����ĿΪNA | |
| C�� | 17 g OH- ������������ĿΪ10NA | |
| D�� | 58.5 g NaCl�������е�Na+������ĿΪNA |
| A�� | ��ͬ��Ԫ����ɵ����� | B�� | ����ʽ��ͬ�ijɷ���ɵ����� | ||
| C�� | ��ͬ�ַ�����ɵ����� | D�� | ��������ͬ��������ɵ����� |
