题目内容
18.在一定温度下,将等物质的量的CO和H2O(g)通入恒容密闭容器中,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),当正逆反应速率相等且不等于零时,下列说法不正确的是( )
| A. | 此时反应达到平衡 | B. | H2的浓度不再改变 | ||
| C. | 升温能使反应速率加快 | D. | CO和H2O完全转化 |
分析 A、当正逆反应速率相等且不等于零时,各物质的量不变;
B、当正逆反应速率相等,所以各物质的浓度保持不变;
C、任何化学反应温度越高反应速率越快;
D、可逆反应不可能完全转化.
解答 解:A、当正逆反应速率相等且不等于零时,说明达平衡状态,故A正确;
B、当正逆反应速率相等,所以各物质的浓度保持不变,所以H2的浓度不再改变,故B正确;
C、任何化学反应温度越高反应速率越快,故C正确;
D、可逆反应不可能完全转化,是反应物和生成物共存的体系,所以既有一氧化碳又有二氧化碳,故D错误;
故选D.
点评 本题考查学生化学反应的可逆性以及平衡的特征知识,属于综合知识的考查,难度不大.

练习册系列答案
相关题目
8.以石油化工为基础的三大合成材料是( )
①陶瓷②塑料③水泥④合成橡胶⑤合成纤维⑥玻璃.
①陶瓷②塑料③水泥④合成橡胶⑤合成纤维⑥玻璃.
| A. | ①②③ | B. | ①③⑥ | C. | ②④⑤ | D. | ③⑤⑥ |
9.2008年北京奥运会“祥云”火炬用的是环保型燃料-丙烷.下列有关说法不正确的是( )
| A. | 奥运火炬燃烧主要是将化学能转变为热能和光能 | |
| B. | 丙烷的沸点比正丁烷高 | |
| C. | 丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的负极 | |
| D. | 丙烷与甲烷属同系物,也无同分异构体 |
13.2014年是门捷列夫诞辰180周年,下列事实不能用元素周期律解释的有( )
| A. | 碱性:KOH>NaOH | B. | 溶解度:SO2>CO2 | ||
| C. | 酸性:HClO4>H2SO4 | D. | 气态氢化物的稳定性:H2O>NH3 |
10.按如图装置进行实验,若图B的X轴表示流入电极的电子的物质的量,则Y轴不可能表示的情况是( )
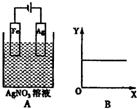

| A. | c (Ag+) | B. | 溶液的pH | C. | Ag棒的质量 | D. | c(NO3-) |
7.氮的最高价氧化物为无色晶体,它由两种离子构成,已知其阴离子构型为平面三角形,则其阳离子的构型和阳离子中氮的杂化方式为( )
| A. | 直线 sp杂化 | B. | V型 sp杂化 | ||
| C. | 三角锥形 sp2杂化 | D. | 平面三角形 sp2杂化 |
 298K时,某容积固定为1L的密闭容器中发生如下可逆反应:A(g)?2B(g)△H=akJ•mol-1.其中B的物质的量浓度随时间变化如图所示.试回答下列问题.
298K时,某容积固定为1L的密闭容器中发生如下可逆反应:A(g)?2B(g)△H=akJ•mol-1.其中B的物质的量浓度随时间变化如图所示.试回答下列问题.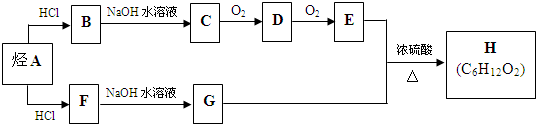
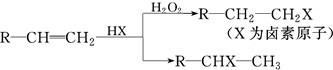
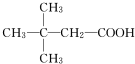 .(用结构简式表示)
.(用结构简式表示) .
.