题目内容
【题目】废气中的H2S通过高温热分解可制取氢气:2H2S(g)![]() 2H2(g)+ S2(g)(正反应吸热)。现在3L密闭容器中,控制不同温度进行H2S分解实验。
2H2(g)+ S2(g)(正反应吸热)。现在3L密闭容器中,控制不同温度进行H2S分解实验。
(1)某温度时,测得反应体系中有气体1.31 mol,反应10 min后,测得气体为l.37 mol,则10 min 内H2的平均生成速率为________________。
(2)某温度时,判断H2S的转化率达到最大值的依据是________(选填编号)。
a.气体的压强不发生变化 b.气体的密度不发生变化
c.单位时间里分解的H2S和生成的H2一样多 d.反应物不再转化为生成物
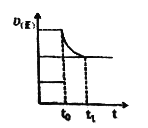
(3)如图所示,该可逆反应在t0时因改变某外界条件而打破原平衡,在t1时达到新的平衡状态,因此推断,t0时改变的外界条件可能是__________________、___________________。
(4)在容器体积不变的情况下,如果要提高H2S的转化率,可采取的一种措施是_____________。
(5)在实验室,若将H2S通入浓硫酸中,发生的化学反应的方程式是:__________。
(6)若将H2S完全燃烧后,并用碳酸钠与碳酸氢钠的混合溶液吸收生成气体SO2,发生如下反应:2Na2CO3+SO2+H2O→ 2NaHCO3+Na2SO3
充分反应后(无CO2逸出),所得溶液组成如表:
物质 | Na2CO3 | NaHCO3 | Na2SO3 |
物质的量(mol) | 2 | 12 | 4 |
则原吸收液中碳酸钠与碳酸氢钠的物质的量之比________________________。
【答案】 0.004 mol/(Lmin) a 升温 增加H2S的浓度(两者顺序可以颠倒) 升温(或分离出H2或或分离出S2) 3H2S+H2SO4(浓)→4S↓+4H2O 5:2
【解析】(1)2H2S(g)![]() 2H2(g)+ S2(g) 物质的量的变化量为1,某温度时,测得反应体系中有气体1.31 mol,反应10 min后,测得气体为l.37 mol,变化量为0.06mol,说明生成的氢气的物质的量为0.12mol,则10 min 内H2的平均生成速率为
2H2(g)+ S2(g) 物质的量的变化量为1,某温度时,测得反应体系中有气体1.31 mol,反应10 min后,测得气体为l.37 mol,变化量为0.06mol,说明生成的氢气的物质的量为0.12mol,则10 min 内H2的平均生成速率为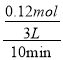 = 0.004 mol/(Lmin) ,故答案为:0.004 mol/(Lmin);
= 0.004 mol/(Lmin) ,故答案为:0.004 mol/(Lmin);
(2)H2S的转化率达到最大值表示反应达到平衡状态。a.该反应前后,气体的物质的量发生变化,压强发生变化,则气体的压强不发生变化时,表示达到了平衡状态,正确;b.容器的体积不变,气体的质量不变,因此气体的密度始终不变,不能说明是否为平衡状态,错误;
c.根据方程式,单位时间里分解的H2S和生成的H2始终一样多,不能说明是否为平衡状态,错误;d.反应物不再转化为生成物,表示反应已经停止,而平衡状态是动态平衡,错误;故选a;
(3)反应在t0时因改变某外界条件而打破原平衡,正反应速率突然增大,然后逐渐减小,说明平衡正向移动,正反应吸热,升高温度,平衡正向移动,增加H2S的浓度,平衡正向移动,t0时改变的外界条件可能是升温或增加H2S的浓度,故答案为:升温或增加H2S的浓度;
(4)在容器体积不变的情况下,如果要提高H2S的转化率,需要使平衡正向移动,根据(3)的分析,升高温度,平衡正向移动,增加H2S的浓度,平衡正向移动,但H2S的转化率减小,其他措施还可以是分离出H2或或分离出S2等,故答案为:升温;
(5)浓硫酸具有强氧化性,将H2S通入浓硫酸中发生氧化还原反应,反应的化学方程式为3H2S+H2SO4(浓)=4S↓+4H2O,故答案为:3H2S+H2SO4(浓)=4S↓+4H2O;
(6)最终溶液中生成的亚硫酸钠为4mol,根据方程式2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3,同时生成碳酸氢钠8mol,消耗碳酸钠8mol,则原溶液中含有碳酸氢钠12mol-8mol=4mol,碳酸钠8mol+2mol=10mol,则原吸收液中碳酸钠与碳酸氢钠的物质的量之比为10:4=5:2,故答案为:5:2。