题目内容
【题目】按第26届国际计量大会重新定义,阿伏加德罗常数(NA)有了准确值6.02214076×1023。下列有关NA的说法正确的是( )
A.28g乙烯与丙烯的混合气体中含有4NA个C-H键
B.标准状况下,3.36LNO2中氧原子数目为0.3NA
C.1L1mol·L-1的CH3COOH溶液与1L0.5mol·L-1的NaOH溶液混合后,CH3COO-的数目为0.5NA
D.理论上,149gNaClO与足量KI溶液反应可得到NA个碘分子
【答案】A
【解析】
A.乙烯和丙烯的通式为(CH)n,乙烯中含有4个C-H键,丙烯含有6个C-H键,都是1个C对应2个C-H键,28g相当于2molCH2,故有4NA个C-H键,故A正确;
B.标况下二氧化氮为液体,3.36L二氧化氮的物质的量不是0.15mol,故B错误;
C.二者混合后溶液中溶质为0.25mol/LCH3COOH和0.25mol/LCH3COONa,由于醋酸的电离程度和醋酸根的水解程度不相等,所以CH3COO-的数目不是0.5NA,故C错误;
D.149gNaClO的物质的量为![]() =2mol,氧化I-时被还原成Cl-,可转移4mol电子,故可以生成2mol碘单质,故D错误;
=2mol,氧化I-时被还原成Cl-,可转移4mol电子,故可以生成2mol碘单质,故D错误;
故答案为A。

 全能测控期末小状元系列答案
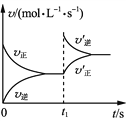
全能测控期末小状元系列答案【题目】一定温度下,10mL0.40molL-1H2O2在MnO2作用下发生反应 :2H2O2 ( aq)=2H2O(l )+O2( g) △H <0, 不同时刻测定生成O2的物质的量如下表所示 :
t/min | 0 | 3 | 6 | 10 | ……. |
n(O2)/mol | 0.0 | 0.0008 | 0.001 | 0.0012 | ……. |
下列叙述不正确的是(溶液体积变化忽略不计)
A.升高温度,可加快H2O2 的分解速率
B.若增大溶液起始浓度,则收集到 0.0 008 mol O2 的时间会小于3 min
C.反应至 6min 时,溶液 中 c(H2O2)=0.2mol L-1
D.反应至 12min 时,H2O2分解率为 65%