题目内容
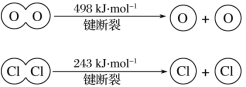
【题目】(1)某反应过程中的能量变化如下图所示:
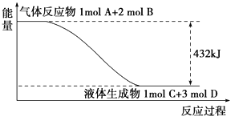
写出该反应的热化学方程式________。
(2)在溶液中进行的化学反应中的物质,其状态标为“aq”,已知1 molHCl在溶液中与足量氢氧化钠反应放出57.3 kJ的热量,用离子方程式写出该反应的热化学方程式:______。
【答案】A(g)+2B(g)=C(l)+3D(l)△H=-432 kJmol-1 H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJmol-1
【解析】
(1)由图可知为放热反应,焓变为负,结合状态及焓变书写热化学方程式;
(2)1molHC1在溶液中与足量氢氧化钠反应放出57.3kJ的热量,可知氢离子与氢氧根离子生成1mol水时放出57.3kJ的热量,据此书写。
(1)从图上可判断反应物总能量高于生成物总能量,反应放热,△H<0,反应物是气态,生成物是液态,则该反应的热化学方程式为A(g)+2B(g)=C(l)+3D(l)△H=-432 kJmol-1;
(2)1 molHCl在溶液中与足量氢氧化钠反应放出57.3 kJ的热量,实质上是1molH+与OH-的中和反应,因此热化学方程式为H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJmol-1。

练习册系列答案
相关题目
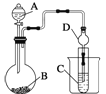
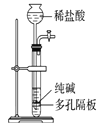
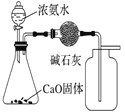
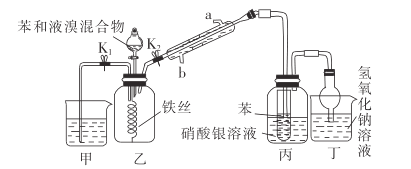
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是( )
选项 | A | B | C | D |
实验 装置 |
|
|
|
|
实验 目的 | 制取少量纯净的CO2气体 | 验证钠和水的反应是放热反应 | 制取并收集干燥纯净的NH3 | 进行喷泉实验 |
A.AB.BC.CD.D