题目内容
【题目】我国部分城市灰霾天占全年一半,引起灰霾的 PM2.5 微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等。通过测定灰霾中锌等重金属的含量,可知目前造成我国灰霾天气的原因主要是交通污染。
(1)Zn2+在基态时核外电子排布式为_____。
(2)NO3-的立体构型是_____。
(3)PM2.5 含有大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有 NOx、O3、CH2=CH—CHO、HCOOH、CH3COOONO2(PAN)等二次污染物。
①下列说法正确的是_____。
A.N2O 结构式可表示为 N=N=O
B.O3 分子呈直线形
C.CH2=CH—CHO 分子中碳原子均采用 sp2 杂化
D.相同压强下,HCOOH 沸点比 CH3OCH3高,说明前者是极性分子,后者是非极性分子
②1 mol PAN 中含σ键数目为_____(用含 NA的式子表示)。
③NO 能被 FeSO4 溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配位数为_____(填数字)。
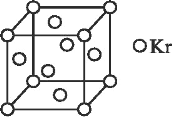
(4)测定大气中 PM2.5 的浓度方法之一是β-射线吸收法,β-射线放射源可用 85Kr,已知 Kr晶体的晶胞结构如图所示,设晶体中与每个 Kr 原子相紧邻的 Kr 原子有 m 个,晶胞中含 Kr
原子为 n 个,则m/n=___(填数字)。
(5)水分子的立体结构是_____,水分子能与很多金属离子形成配合物,其原因是在氧原子上有__________。
(6)冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心所示原子位于立方体的 顶点或面心,实心球所示原子位于立方体内)类似。每个冰晶胞平均占有_____个水分子。 冰晶胞与金刚石晶胞微粒排列方式相同的原因是_________。

【答案】1s22s22p63s23p63d10平面三角形AC0NA63V 形孤电子对8C 原子与 O 原子都为 sp3 杂化,且氢键和共价键都具有方向性和饱和性
【解析】
(1)Zn是30号元素,其原子核外有30个电子,失去两个电子生成锌离子,Zn2+基态核外有28个电子,根据构造原理书写其核外电子排布式;
(2)根据VSEPR理论和杂化轨道理论判断NO3-的空间构型;
(3)①A、N2O与CO2互为等电子体,二者形成的化学键相似,据此答题;B、O3与SO2互为等电子体,据此答题;C、CH2=CH-CHO中每个碳原子均形成两个单键和一个双键,故均为sp2杂化,据此答题;D、HCOOH分子间能形成氢键,CH3OCH3不能形成分子间氢键,据此答题;
②一个单键就是一个σ键,一个双键中含有一个σ键,一个π键;
③配体位于方括号中,由1个NO和5个H2O构成。
(4)以顶点为计算,与之相邻的最近的Kr位于三个面心上,而顶点的原子为8个立方体共有,每个面心上的Kr为两个立方体共有,故与每个Kr原子相紧邻的Kr原子有3×4=12,晶胞中含Kr原子为8×1/8+6×1/2=4,然后求出比值;
(5)根据σ键数目和孤电子对数判断分子的立体构型;水分子能与很多金属离子形成配合物,其原因是在氧原子上有孤对电子,金属离子有空轨道,能形成配位键;
(6)由图可知,水位于晶胞的顶点、面心和晶胞内,利用均摊法计算;金刚石中,C原子为sp3杂化,而冰晶胞与金刚石晶胞微粒排列方式相同,说明C原子与O原子都为sp3杂化,且氢键和共价键都具有方向性和饱和性。
(1)Zn为30号元素,所以Zn2+在基态时核外电子排布式为:1s22s22p63s23p63d10或[Ar]3d10;
因此,本题正确答案是:1s22s22p63s23p63d10;
(2)对于NO3-,根据VSEPR理论,中心N原子的配位原子数3,孤电子对数为0,则价电子对数为3+0=3,根据杂化轨道理论,中心N原子为sp2杂化,则其空间构型为平面三角形;
因此,本题正确答案是:平面三角形;
(3)①A、N2O与CO2互为等电子体,二者形成的化学键相似,故N2O结构式可表示为N=N=O,A正确;
B、O3与SO2互为等电子体,为V形分子,B错误;
C、CH2=CH-CHO中每个碳原子均形成两个单键和一个双键,故均为sp2杂化,C正确;
D、HCOOH分子间可以形成氢键,CH3OCH3分子间只有范德华力,氢键的作用强于范德华力,所以HCOOH沸点比CH3OCH3高,与分子的极性无关,D错误。
答案选AC;
②PAN中所有单键均为σ键,双键中有一个为σ键,-NO2的结构为![]() ,所以PAN(CH3COOONO2)分子中含有10个σ键,则1mo1PAN含σ键数目为10 NA(或10×6.02×1023或6.02×1022)。
,所以PAN(CH3COOONO2)分子中含有10个σ键,则1mo1PAN含σ键数目为10 NA(或10×6.02×1023或6.02×1022)。
③配体位于方括号中,由1个NO和5个H2O构成,则配位数为6。
因此,本题正确答案是:AC;10NA;6;
(4)根据均摊法,以顶点计算,与之相邻最近的Kr位于三个面心上,而顶点的原子为8个立方体共有,每个面心上的Kr为两个立方体共有,故最近的Kr为3×8/2=12,晶胞中Kr有8×1/8+6×1/2=4,两者比值为12:4=3。
因此,本题正确答案是:3;
(5)水分子中含有2个σ键,孤电子对数=![]() =2,所以水分子的立体构型为V型,水分子能与很多金属离子形成配合物,其原因是在氧原子上有孤对电子,金属离子有空轨道,能形成配位键;
=2,所以水分子的立体构型为V型,水分子能与很多金属离子形成配合物,其原因是在氧原子上有孤对电子,金属离子有空轨道,能形成配位键;
因此,本题正确答案是:V形;孤电子对;
(6)每个冰晶胞平均含有水分子数为:8×![]() +6×
+6×![]() +4=8(其中顶点为8个,面心为6个,晶胞内有4个);金刚石中,C原子为sp3杂化,而冰晶胞与金刚石晶胞微粒排列方式相同,说明C原子与O原子都为sp3杂化,且氢键和共价键都具有方向性和饱和性;
+4=8(其中顶点为8个,面心为6个,晶胞内有4个);金刚石中,C原子为sp3杂化,而冰晶胞与金刚石晶胞微粒排列方式相同,说明C原子与O原子都为sp3杂化,且氢键和共价键都具有方向性和饱和性;
因此,本题正确答案是:8 ;C原子与O原子都为sp3杂化,且氢键和共价键都具有方向性和饱和性。

【题目】用如下图装置实验,下列实验现象预期及相应结论均正确的是
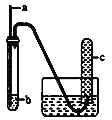
a | b | 实验现象预期 | 结论 | |
A | 铁丝 | HCl酸化的H2O2 | c中收集到无色气体 | 铁丝催化H2O2分解 |
B | 铜丝 | 浓硝酸 | c中收集到红棕色气体 | 硝酸有强氧化性 |
C | 生铁 | NaCl溶液 | 导管处发生倒吸 | 生铁发生吸氧腐蚀 |
D | 木条 | 浓硫酸 | 木条变黑 | 浓硫酸有强氧化性 |
A. A B. B C. C D. D