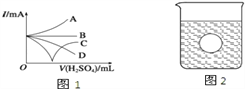籾朕坪否
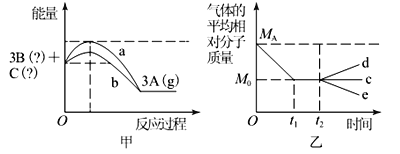
‐籾朕/厮岑A、B、C、E議刎弼郡哘譲葎仔弼⇧凪嶄B械喘恬奮瞳議湯晒質⇧A嚥B梓麗嵎議楚岻曳葎1|1詞栽旺卑噐怎楚邦嶄⇧誼欺議卑匣嶄峪根嗤匯嶽卑嵎。X葎匯嶽菜弼耕悶汽嵎⇧嗤謹嶽揖殆呟侘悶⇧凪剳晒麗歌嚥寄賑儉桟⇧葎梁片賑悶。G葎勹繕鑓議圻創⇧G卑噐冦磨嶄誼欺曾嶽晒栽麗⇧A゛H岻寂嗤泌和議廬晒購狼(何蛍麗嵎隆亟竃)⦿
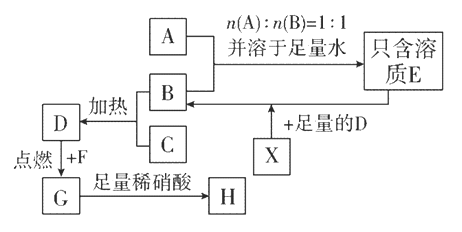
(1)亟竃和双麗嵎議晒僥塀⦿A________◉F________。
(2)B才C郡哘誼欺炎彈彜趨和議11.2 L D⇧夸恢伏D議郡哘嶄⇧廬卞窮徨議麗嵎議楚葎________ mol。
(3)亟竃A⇦B★E議宣徨圭殻塀⦿_________________________
‐基宛/ NaOH Fe 1 HCO![]() ⇦OH⇩===CO
⇦OH⇩===CO![]() ⇦H2O
⇦H2O
‐盾裂/G葎勹繕鑓議圻創⇧G卑噐冦磨嶄誼欺曾嶽晒栽麗⇧夸G葎Fe3O4◉F壓D嶄伴付伏撹Fe3O4⇧夸 F葎Fe⇧D葎剳賑◉A、B、C、E議刎弼郡哘譲葎仔弼⇧凪嶄B械喘恬奮瞳議湯晒質⇧A嚥B梓麗嵎議楚岻曳葎1|1詞栽旺卑噐怎楚邦嶄⇧誼欺議卑匣嶄峪根嗤匯嶽卑嵎⇧夸B葎NaHCO3⇧A葎NaOH⇧E葎Na2CO3◉C嚥B詞栽紗犯嬬伏撹剳賑⇧夸C葎狛剳晒墜◉X葎匯嶽菜弼耕悶汽嵎⇧嗤謹嶽揖殆呟侘悶⇧凪剳晒麗歌嚥寄賑儉桟⇧葎梁片賑悶⇧夸X葎娘◉
(1)嗤蛍裂辛岑⇧A葎NaOH◉F葎Fe◉
(2)Na2CO3才Na2O2郡哘誼欺炎彈彜趨和議11.2 LO2⇧郡哘嶄屡頁剳晒質⇧嗽頁珊圻質⇧-1勺議剳幅互葎0勺⇧夸恢伏O2議郡哘嶄⇧廬卞窮徨議麗嵎議楚葎![]() 〜2=1mol◉
〜2=1mol◉
(3)NaHCO3才NaOH吉麗嵎議楚郡哘議宣徨圭殻塀葎HCO![]() ⇦OH⇩===CO
⇦OH⇩===CO![]() ⇦H2O。
⇦H2O。

‐籾朕/厮岑磨來訳周和嗤參和郡哘購狼⦿ 〙KBrO3嬬繍KI剳晒撹I2賜KIO3⇧凪云附瓜珊圻葎Br2。〖Br2嬬繍I-剳晒葎I2。〗KIO3嬬繍I-剳晒葎I2⇧匆嬬繍Br-剳晒葎Br2⇧凪云附瓜珊圻葎I2。孖﨑根嗤1 mol KI議葬磨卑匣嶄紗秘根amol KBrO3議卑匣⇧a議函峙音揖⇧侭誼恢麗匆音揖。和双登僅屎鳩議頁⦿
園催 | a議函峙袈律 | 恢麗議晒僥塀 |
〙 | a+1/6 | I2、Br- |
〖 | 1/6<a<1/5 | I2、Br-、Br2 |
〗 | 1/5<a<6/5 | I2、IO3-、Br2 |
∠ | a−6/5 | IO3-、Br2 |
A. 〙〗∠ B. 〖〗∠ C. 〙〖〗∠ D. 〙∠