题目内容
3.下列离子或分子在指定介质中能大量共存的是( )| A. | 硝酸亚铁溶液中:Al3+、H+、SO42-、Cl-、CO32- | |
| B. | 透明溶液中:Cu2+、Fe3+、NH4+、NO3-、SO42- | |
| C. | 强酸性溶液中:CH3CH2OH、Mg2+、MnO4-、SiO32- | |
| D. | 含有大量ClO-的溶液中:K+、OH-、I-、SO32- |
分析 A.离子之间结合生成水、气体或沉淀;
B.该组离子之间不反应;
C.强酸溶液中不能大量存在SiO32-,且离子之间发生氧化还原反应;
D.离子之间发生氧化还原反应.
解答 解:A.H+、CO32-结合生成水、气体,Al3+、Fe2+分别与CO32-结合生成沉淀,不能大量共存,故A错误;
B.该组离子之间不反应,可大量共存,故B正确;
C.强酸溶液中不能大量存在SiO32-,且CH3CH2OH、H+、MnO4-发生氧化还原反应,不能大量共存,故C错误;
D.ClO-分别与I-、SO32-发生氧化还原反应,不能大量共存,故D错误;
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
13.下列关于气体和溶液的叙述正确的是( )
| A. | 0.5 mol•L-1 CuCl2溶液中含有3.01×1023个Cu2+ | |
| B. | 标准状况下,2.24 L CO2气体含有1.81×1023个氧原子 | |
| C. | 48 g O3气体含有6.02×1023个O3分子 | |
| D. | 标准状况下,33.6 L H2O含有1.5NA个H2O分子 |
14.已知外电路中,电子由铜流向a极.有关图中装置分析合理的一项是( )
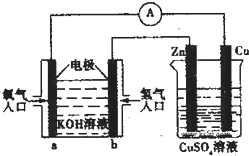

| A. | 一段时间后锌片质量减少 | |
| B. | 该装之中Cu极为正极 | |
| C. | b极的电极反应式:H2-2e-═2H+ | |
| D. | 当铜片的质量变化为12.8g时,a极上消耗的 O2在标况下的体积为2.24L |
11.在下列变化中,需要加入合适的氧化剂才能实现的是( )
| A. | Fe→Fe3+ | B. | CO2→CO | C. | Na2O2→O2 | D. | CuO→Cu2+ |
18.X、Y、Z三种物质中含同种元素,在一定条件下可以实现如图所示转化,下列推断不正确的是( )
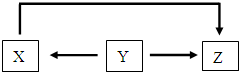

| A. | 若Y为氧化铝,则Y 生成X的条件是“通电” | |
| B. | 若X为硫单质,则Y 可能为硫化氢 | |
| C. | 若Z为硝酸,则X可能为一氧化氮 | |
| D. | 若Z为硝酸铁,则Y一定为铁单质 |
15.下列关于物质在氧气中燃烧的现象的叙述中,正确的是( )
| A. | 木炭在氧气中燃烧,产生大量白烟 | |
| B. | 红磷在空气中燃烧,产生苍白色火焰 | |
| C. | 镁条在空气中燃烧发出耀眼白光,生成黑色固体 | |
| D. | 硫在氧气中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体 |
12.下列说法正确的是( )
| A. | 摩尔是国际七个基本物理量之一 | |
| B. | 摩尔质量等于相对分子质量或相对原子质量 | |
| C. | 标准状况下,任何气体的摩尔体积都约为22.4L | |
| D. | 1mol某种微粒含有的微粒数等于0.012kg12C所具有的碳原子数 |