题目内容
8.无水AlCl3易升华,可用作有机合成的催化剂等,工业上由铝土矿(主要成分是Al2O3和Fe2O3,还含有少量的SiO2 )和石油焦(主要成分是C)为原料制备无水AlCl3:2Al2O3+6Cl2═4AlCl3+3O2回答以下问题:
(1)加入焦炭后的化学反应可表示为Al2O3+C+Cl2 $\stackrel{加热}{→}$AlCl3+X↑,设计实验确定气体X的成分:气体X可能为CO、CO2或两者的混合物,将生成气体依次通过澄清石灰水、灼热的CuO粉末,如溶液变浑浊,则X中存在CO2,如黑色CuO粉末变成红色粉末,则X中存在CO.
(2)在提纯AlCl3粗产品时,需加入少量铝粉,可使熔点较低的FeCl3转化为熔点较高的FeCl2,从而避免在AlCl3中混入铁的氯化物.该反应的化学方程式为Al+3FeCl3$\frac{\underline{\;\;△\;\;}}{\;}$AlCl3+3FeCl2.
(3)为测定制得的无水AlCl3产品(含FeCl3杂质)的纯度,称取16.25g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32g.
①过程涉及的离子方程式Fe3++3OH-═Fe(OH)3↓、Al3++4OH-═AlO2-+2H2O.
②AlCl3产品的纯度为96%.
分析 (1)根据反应方程式可知,气体X可能为一氧化碳、二氧化碳或者二者混合物,可以利用澄清石灰水检验二氧化碳,利用灼热的氧化铜检验一氧化碳,据此涉及实验方案;
(2)根据题中信息可知,反应物为Al和FeCl3,反应产物为氯化铝和FeCl2,据此写出反应的化学方程式;
(3)①根据铝离子、铁离子与过量的氢氧根离子反应生成偏铝酸根离子、氢氧化铁沉淀写出反应的离子方程式;
②残留固体质量为0.32g为氧化铁,可以计算出铁离子的物质的量及氯化铁的质量,最后根据总质量计算出氯化铝的纯度.
解答 解:(1)从Al2O3+C+Cl2$\stackrel{△}{→}$AlCl3+X↑可以看出X为CO、CO2或两者的混合物,确定气体X的成分,就是检验CO、CO2的存在,检验方法为:气体X可能为CO、CO2或两者的混合物,将生成气体依次通过澄清石灰水、灼热的CuO粉末,如溶液变浑浊,则X中存在CO2,如黑色CuO粉末变成红色粉末,则X中存在CO,
故答案为:气体X可能为CO、CO2或两者的混合物,将生成气体依次通过澄清石灰水、灼热的CuO粉末,如溶液变浑浊,则X中存在CO2,如黑色CuO粉末变成红色粉末,则X中存在CO;
(2)铝将氯化铁还原为氯化亚铁,反应的化学方程式为:Al+3FeCl3$\frac{\underline{\;\;△\;\;}}{\;}$AlCl3+3FeCl2,
故答案为:Al+3FeCl3$\frac{\underline{\;\;△\;\;}}{\;}$AlCl3+3FeCl2;
(3)①该制取过程中涉及的离子方程式有AlCl3与过量的NaOH溶液的反应和FeCl3与NaOH溶液的反应,反应的离子方程式为:Fe3++3OH-═Fe(OH)3↓;Al3++4OH-═AlO2-+2H2O,
故答案为:Fe3++3OH-═Fe(OH)3↓;Al3++4OH-═AlO2-+2H2O;
②0.32 g残留固体质量是Fe2O3,则铁离子的物质的量为:n(Fe3+)=0.004 mol,氯化铁的质量为:m(FeCl3)=162.5g/mol×0.004mol=0.65 g,混合物中氯化铝的质量为:m(AlCl3)=16.25g-0.65g=15.6 g,所以AlCl3产品的纯度为:$\frac{15.6g}{16.25g}$×100%=96%,
故答案为:96%.
点评 本题考查了物质的分离与提纯、探究物质组成与含量等知识,题目难度中等,充分考查了学生对所学知识的掌握情况,试题有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

 阅读快车系列答案
阅读快车系列答案| A. | 20g D2O含有的电子数为10NA | |
| B. | 常温下,4g CH4含有NA个C-H共价键 | |
| C. | 标准状况下,5.6 L四氯化碳含有的分子数为0.25NA | |
| D. | 1mol Na2O2与CO2完全反应时转移电子数为NA |
| A. | “海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化 | |
| B. | 蒙古牧民喜欢用银器盛放鲜牛奶有其科学道理:用银器盛放鲜牛奶,溶入的极微量的银离子,可杀死牛奶中的细菌,防止牛奶变质 | |
| C. | “乙醇汽油”因油价上涨而被广泛使用.它是指在汽油里加入适量乙醇混合而成的一种燃料,它是一种新型的化合物 | |
| D. | 某雨水样品采集后放置一段时间,pH值由4.68变为4.28,是因为水中溶解了较多的CO2 |
| A. | 硝酸亚铁溶液中:Al3+、H+、SO42-、Cl-、CO32- | |
| B. | 透明溶液中:Cu2+、Fe3+、NH4+、NO3-、SO42- | |
| C. | 强酸性溶液中:CH3CH2OH、Mg2+、MnO4-、SiO32- | |
| D. | 含有大量ClO-的溶液中:K+、OH-、I-、SO32- |
| A. | 氢气 | B. | 太阳能 | C. | 天然气 | D. | 石油 |
| A. | 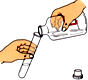 加入药品 | B. | 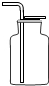 收集气体 | C. | 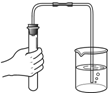 检查装置气密性 | D. | 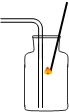 气体验满 |
| A. | 标准状况下72mL水 | B. | 80g CO2 | ||
| C. | 标准状况下44.8L氨气 | D. | 3.01×1023个氢分子 |
| A. | 用pH试纸测量新制氯水的pH | |
| B. | 用10mL量筒量取5.2mL的盐酸 | |
| C. | 用托盘天平称取25.20gNaCl | |
| D. | 用量筒量取20mL0.5000 mol•L-1H2SO4溶液于烧杯中,加水80 mL,配制成0.1000 mol•L-1H2SO4溶液 |