题目内容
2.水在很多的反应中,起到极其重要的作用.根据下面水参与的反应,回答:①2F2+2H2O═4HF+O2
②2Na2O2+2H2O═4NaOH+O2↑
③2Na+2H2O═2NaOH+H2↑
④2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑
水只作氧化剂的是③ (填写序号,下同);水只作还原剂的是①;水既作氧化剂,又作还原剂的是④.
分析 水中H元素的化合价降低,水作氧化剂;水中O元素的化合价升高,则水作还原剂,以此来解答.
解答 解:①2F2+2H2O═4HF+O2中,水中O元素的化合价升高,则水作还原剂;
②2Na2O2+2H2O═4NaOH+O2↑中,水中H、O元素的化合价均不变;
③2Na+2H2O═2NaOH+H2↑中,水中H元素的化合价降低,则水为氧化剂;
④2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑中,水中H元素化合价降低、O元素的化合价升高,则水既作氧化剂,又作还原剂,
故答案为:③;①;④.
点评 本题考查氧化还原反应,为高频考点,把握氧化还原反应中元素的化合价变化及氧化还原反应基本概念为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
10.能防止贫血的一种元素是( )
| A. | 铁 | B. | 碘 | C. | 铜 | D. | 镁 |
17.下列各组物质,前者属于电解质,后者属于非电解质的是( )
| A. | NaCl晶体、CO2 | B. | 铜、二氧化硫 | ||
| C. | Na2CO3溶液、酒精 | D. | 熔融的KNO3、硫酸溶液 |
7.2005年10月12日我国用长征二号F型火箭成功发射了神舟“六号”载人飞船,并于10月17日圆满着陆.标志着我国载人航天又有新的突破.长征二号F型火箭用的燃料是液态的偏二甲基肼(C2H8N2),氧化剂是液态的N2O4,已知1.5g火箭燃料偏二甲基肼完全燃烧生成氮气,二氧化碳和液态水放出热量50kJ.下列说法不正确的是( )
| A. | 燃料在火箭发动机中燃烧是将化学能主要转变为热能和机械能 | |
| B. | 偏二甲基肼在四氧化氮中的燃烧反应是放热反应 | |
| C. | 该反应中偏二甲基肼和四氧化氮总能量小于二氧化碳、氮气和水的总能量 | |
| D. | 燃烧时的总反应为:C2H8N2+2N2O4$\stackrel{点燃}{→}$2CO2+3N2+4H2O |
14.磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性.制备时将FeSO4和Fe2(SO4)3的溶液等物质的量混合,滴入稍过量的氢氧化钠溶液,随后加入油酸钠溶液,即可生成黑色的分散质粒子直径在5.5nm~36nm(1nm=10-9m)的磁流体.下列说法正确的是( )
| A. | 所得的分散系属于溶液 | B. | 所得的分散系能产生丁达尔效应 | ||
| C. | 所得的分散系不能通过滤纸 | D. | 磁流体微粒的直径比Fe2+小 |
11.如表实验操作正确的是( )
| 编号 | 实验 | 操作 |
| A | 实验室用自来水制备蒸馏水 | 将自来水倒入烧杯中,小心给烧杯加热 |
| B | 配制一定浓度的氯化钾溶液100mL | 将称好的氯化钾固体放入100mL容量瓶中,加水溶解,振荡摇匀,定容 |
| C | 检验溶液中是否含SO42- | 先加入稀盐酸,无明显现象,再加入BaCl2溶液 |
| D | 取出分液漏斗中的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
| A. | A | B. | B | C. | C | D. | D |
19.电解质和非电解质是对化合物的一种分类方式.下列关于电解质的说法正确的是( )
| A. | 液态HCl不导电,所以AgCl不是电解质 | |
| B. | AgCl在水溶液中难导电,但熔融状态下能导电,所以AgCl是电解质 | |
| C. | 电解质一定能导电,能导电的物质一定属于电解质 | |
| D. | CO2溶于水形成的济液能导电,所以CO2是电解质 |
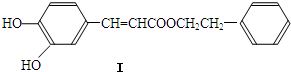
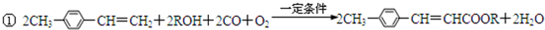
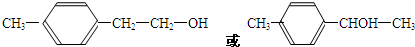 (写1种);由IV生成II的反应条件为NaOH醇溶液,加热.
(写1种);由IV生成II的反应条件为NaOH醇溶液,加热.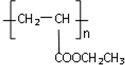 可用于制备涂料,其单体结构简式为CH2=CHCOOCH2CH3.利用类似反应①的方法,仅以乙烯为有机物原料合成该单体,涉及的反应方程式为(提示:共有两步反应方程式)CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{催化剂}{→}$2CH2=CHCOOCH2CH3+2H2O.
可用于制备涂料,其单体结构简式为CH2=CHCOOCH2CH3.利用类似反应①的方法,仅以乙烯为有机物原料合成该单体,涉及的反应方程式为(提示:共有两步反应方程式)CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{催化剂}{→}$2CH2=CHCOOCH2CH3+2H2O.