题目内容
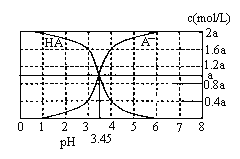
在常温下,0.1000mol·L-1Na2CO3溶液25mL 用0.1000mol·L-1盐酸滴定,其滴定曲线如图6。对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是
| A.a点:c(CO2-3)>c(HCO-3)>c(OH-) |
| B.b点:5c(Cl-)>4c(HCO-3)+4c(CO2-3) |
| C.c点:c(OH-)=c(H+)+c(HCO-3)+2c(H2CO3) |
| D.d点:c(H+)=2c(CO2-3)+c(HCO-3)+c(OH-) |
B
解析试题分析:A、a点为Na2CO3和NaHCO3等量混合液,以Na2CO3第一步水解为主,故c(HCO-3)>c(CO2-3)>c(OH-),错误;B、b点为Na2CO3和NaHCO3混合液,有物料守衡式为5c(Cl-)=4c(H2CO3)+4c(HCO-3)+4c(CO2-3),正确;C、c点为NaHCO3溶液,质子守恒式为c(OH-)+c(CO2-3)=c(H+)+c(H2CO3),错误;D、d点位NaCl和溶解的CO2溶液,电荷守衡为c(H+)+c(Na+)=2c(CO2-3)+c(HCO-3)+c(OH-)+c(Cl-),其中c(Na+)=c(Cl-),故有c(H+)=2c(CO2-3)+c(HCO-3)+c(OH-),正确。
考点:考查溶液中微粒浓度关系的有关问题。

练习册系列答案
 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
下列各溶液中,微粒的物质的量浓度关系表述正确的是
| A.0.1 mol/LNa2CO3溶液中:c(Na+)=(HCO3-)+c(H2CO3)+2c(CO32-) |
| B.常温下pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7 |
| C.将0.2mol/LNaA溶液和0.1 mol·L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) |
| D.pH=l2的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等 |
为比较盐酸与醋酸的酸性强弱,下列方案不可行的是(均在常温下测定)
| A.比较等体积、等pH值的两种溶液的导电性 |
| B.比较等物质的量浓度的氯化钠与醋酸钠溶液的pH值 |
| C.比较等体积、等pH值的两种溶液与过量锌粉反应产生氢气的量 |
| D.比较等体积、等物质的量浓度的两种溶液稀释相同倍数后的pH变化 |
有关CaCO3的溶解平衡的说法中,不正确的是
| A.CaCO3沉淀析出和沉淀溶解不断进行,但速率相等 |
| B.CaCO3难溶于水,其饱和溶液几乎不导电,属于弱电解质溶液 |
| C.升高温度,CaCO3沉淀的溶解度增大 |
| D.向CaCO3沉淀中加入纯碱固体,CaCO3的溶解量降低 |
25℃时,下列各项分别由等体积0.1 mol·L-1的两种溶液混合,有关混合后的溶液说法不正确的是( )
| A.Ba(OH)2溶液与Na2SO4溶液:pH="13" |
| B.醋酸与CH3COONa溶液:c(Na+)+c(H+)= c(CH3COO-)+c(OH-) |
| C.Na2CO3溶液与NaHCO3溶液:2c(Na+) = 3c(CO32-)+3c(HCO3-)+3c(H2CO3) |
| D.Na2CO3溶液与NaOH溶液: c(Na+)>c(CO32-)>c(OH-)>c(H+) |
常温下,下列说法正确的是
| A.往CH3COOH溶液中加水,c(OHˉ)和c(H+)均增大 |
| B.物质的量浓度均为0.1mol?Lˉ1的CH3COOH溶液和NaOH溶液等体积混合,c(Na+)>c(CH3COOˉ) |
| C.某浓度的氯化铵溶液中存在c(NH4+)>c(Clˉ)>c(H+)> c(OHˉ) |
| D.在pH=4的氯化铵溶液中c(H+)+ c(NH4+)=" c(Clˉ)+" c(OHˉ) |