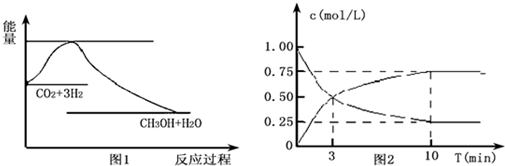
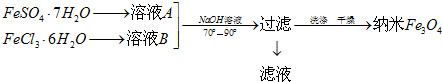
题目内容
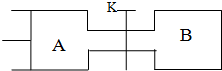
9.如图,A中有一可自由移动的活塞,关闭开关K,先向B中充入2molX和2molY,再向A中充入1molX和1molY.开始时A、B的体积都为aL,在相同的温度和有催化剂存在的条件下,两容器中都开始发生下述反应:X(g)+Y(g)?2Z(g)+W(g),反应达到平衡时,A的体积为1.2aL,则
(1)A中X的转化率a(A)=40%;
(2)A、B中X的转化率a(A)>a(B)(填“<”“=”“>”).
(3)打开开关K,保持温度不变,再达平衡时,A的体积为2.6 L (连通管中气体体积不计).
分析 (1)A为恒温恒压,利用体积之比等于物质的量之比求出平衡时A中混合气体的物质的量,由方程式可知1molX反应时混合气体物质的量增大1mol,即消耗的X的物质的量等于混合气体物质的量增大量,进而计算X的转化率;
(2)A为恒温恒压,B为恒温恒容,随反应进行B中压强增大,故平衡时A中容器压强小于B中压强,B可以等效为在A的基础上增大压强,平衡逆向移动;
(3)打开开关K,保持温度不变,再达平衡时,等效为开始加入3molX、3molY到达的平衡,恒温恒压下与A中平衡为等效平衡,反应物转化率不变,平衡时混合气体总物质的量为A中2倍,恒温恒压下压强之比等于物质的量之比,进而计算开始加入3molX、3molY到达的平衡时总体积,减去容器B的体积即为A容器体积.
解答 解:(1)A为恒温恒压,反应达到平衡时,A的体积为1.2aL,则平衡时混合气体总物质的量为(1+1)mol×$\frac{1.2aL}{aL}$=2.4mol,由方程式可知1molX反应时混合气体物质的量增大1mol,则消耗的X的物质的量为(2.4-2)mol=0.4mol,故X的转化率为$\frac{0.4mol}{1mol}$×100%=40%,
故答案为:40%;
(2)A为恒温恒压,B为恒温恒容,随反应进行B中压强增大,故平衡时A中容器压强小于B中压强,B可以等效为在A的基础上增大压强,平衡逆向移动,B中X的转化率小于A中X的转化率,即a(A)>a(B),
故答案为:>;
(3)打开开关K,保持温度不变,再达平衡时,等效为开始加入3molX、3molY到达的平衡,恒温恒压下与A中平衡为等效平衡,反应物转化率不变,平衡时混合气体总物质的量为A中2倍,恒温恒压下压强之比等于物质的量之比,则开始加入3molX、3molY到达的平衡时总体积为1.2aL×2=3.6aL,故B容器体积为3.6aL-aL=2.6aL,
故答案为:2.6a.
点评 本题考查化学平衡计算,涉及等效平衡问题,较好的考查学生分析解决问题能力,关键是等效平衡途径的建立,难度中等.

 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案| A. | 在水中溶解性:Na2CO3>NaHCO3 | |
| B. | 热稳定性:Na2CO3>NaHCO3 | |
| C. | 与相同浓度的盐酸反应的速度:Na2CO3>NaHCO3 | |
| D. | Na2CO3与NaHCO3可以相互转化 |
| A. | 40% | B. | 50% | C. | 80% | D. | 100% |
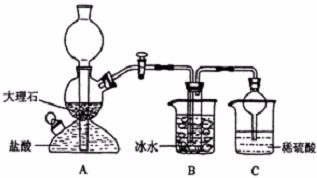
(1)A装置中所发生反应的离子方程式为:CaCO3+2H+=Ca2++CO2+H2O.C装置中稀硫酸的作用为:吸收从B装置中的试管内逸出的氨气,减少对环境的污染.
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在A与B装置之间(填写字母)连接一个盛有饱和NaHCO3溶液 的洗气装置,其作用是除去CO2中混合的HCl气体.
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为60%.
| A. | 直接用酒精灯的外焰加热蒸发皿 | |
| B. | 加热过程中不断用玻璃棒搅拌 | |
| C. | 加热到液体全部消失 | |
| D. | 蒸发皿中出现多量晶体、少量液体时,停止加热,利用蒸发皿的余热烘干 |