题目内容
下列关于金属元素特征的叙述正确的是( )
①金属元素的原子只有还原性,离子只有氧化性;
②金属元素在化合物中一般显正价;
③金属阳离子被还原不一定得到金属单质;
④金属元素不可能存在于阴离子中;
⑤常温下,金属单质中铁和铝均能溶于浓硫酸和浓硝酸;
⑥金属元素由化合态变为游离态一定被还原.
①金属元素的原子只有还原性,离子只有氧化性;
②金属元素在化合物中一般显正价;
③金属阳离子被还原不一定得到金属单质;
④金属元素不可能存在于阴离子中;
⑤常温下,金属单质中铁和铝均能溶于浓硫酸和浓硝酸;
⑥金属元素由化合态变为游离态一定被还原.
| A、①④⑥ | B、②③⑥ |
| C、①④⑤⑥ | D、②③⑤⑥ |
考点:金属的通性
专题:元素及其化合物
分析:①金属单质在反应中只能失去电子,亚铁离子既有氧化性又有还原性;
②因金属元素在反应中失去电子,则化合价一定升高;
③处于高价态的金属,如三价铁离子,能够被还原成亚铁离子进行判断;
④偏铝酸根离子、高锰酸根离子中含有金属元素;
⑤常温下浓硫酸、浓硝酸均能使铁钝化,生成致密的氧化膜阻止反应的进一步发生;
⑥根据金属元素由化合态变为游离态,元素化合价必定降低;
②因金属元素在反应中失去电子,则化合价一定升高;
③处于高价态的金属,如三价铁离子,能够被还原成亚铁离子进行判断;
④偏铝酸根离子、高锰酸根离子中含有金属元素;
⑤常温下浓硫酸、浓硝酸均能使铁钝化,生成致密的氧化膜阻止反应的进一步发生;
⑥根据金属元素由化合态变为游离态,元素化合价必定降低;
解答:
解:①金属单质在反应中只能失去电子,但处于中间价态的金属离子既有氧化性又有还原性,如亚铁离子既有氧化性又有还原性,故①错误;
②金属元素在反应中失去电子,则化合价一定升高,所以金属元素在化合物中一定显正价,故B正确;
③处于高价态的金属,如三价铁离子,能够被还原成亚铁离子,所以金属阳离子被还原不一定得到金属单质,故③正确;
④金属元素可能存在于阴离子中,如偏铝酸根离子、高锰酸根离子,故④错误;
⑤常温下浓硫酸、浓硝酸均能使铁钝化,生成致密的氧化膜阻止反应的进一步发生,所以铁和铝不能溶于浓硫酸和浓硝酸,故⑤错误;
⑥金属元素由化合态变为游离态,元素化合价必定降低,一定被还原,故⑥正确;
故选B.
②金属元素在反应中失去电子,则化合价一定升高,所以金属元素在化合物中一定显正价,故B正确;
③处于高价态的金属,如三价铁离子,能够被还原成亚铁离子,所以金属阳离子被还原不一定得到金属单质,故③正确;
④金属元素可能存在于阴离子中,如偏铝酸根离子、高锰酸根离子,故④错误;
⑤常温下浓硫酸、浓硝酸均能使铁钝化,生成致密的氧化膜阻止反应的进一步发生,所以铁和铝不能溶于浓硫酸和浓硝酸,故⑤错误;
⑥金属元素由化合态变为游离态,元素化合价必定降低,一定被还原,故⑥正确;
故选B.
点评:本题考查金属元素的性质,熟悉常见的金属单质及金属对应的离子是解答本题的关键,难度不大.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
下列各组物质,其中属于同系物的是( )
(1)乙烯和苯乙烯 (2)丙烯酸和油酸 (3)乙醇和丙二醇 (4)丁二烯与异戊二烯
(5)蔗糖与麦芽糖.
(1)乙烯和苯乙烯 (2)丙烯酸和油酸 (3)乙醇和丙二醇 (4)丁二烯与异戊二烯
(5)蔗糖与麦芽糖.
| A、(1)(2)(3)(4) |
| B、(2)(4) |
| C、(1)(2)(4)(5) |
| D、(1)(2)(4) |
下列化学用语正确的是( )
A、聚丙烯的结构简式为: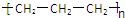 |
B、丙烷分子的比例模型为: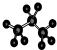 |
| C、甲醛的结构简式:HCHO |
D、羟基的电子式: |
下列关于元素周期律的叙述正确的是( )
| A、随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 |
| B、元素性质的周期性变化是指原子核外电子排布、原子半径及元素主要化合价的周期性变化 |
| C、随着元素原子序数的递增,原子半径从小到大(稀有气体除外)发生周期性变化 |
| D、在元素周期表中有些元素既表现出一定的金属性又表现出一定的非金属性 |
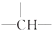 和一个-Cl,它的可能结构分别是
和一个-Cl,它的可能结构分别是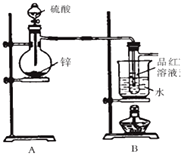 已知实验室制取氯气是用二氧化锰和浓盐酸反应的原理,在收集时,若是用排水法,可能会损失部分氯气.
已知实验室制取氯气是用二氧化锰和浓盐酸反应的原理,在收集时,若是用排水法,可能会损失部分氯气.