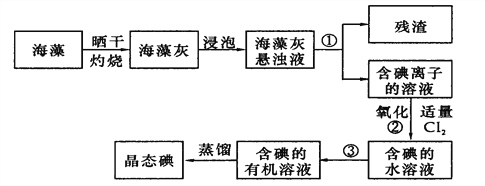
题目内容
【题目】Ⅰ.实验室可以用二氧化锰和浓盐酸反应制取氯气,方程式如下:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,下图是某学生设计的试验室制备干燥Cl2的实验装置图,根据图中的装置和有关试剂回答下列问题:
MnCl2+Cl2↑+2H2O,下图是某学生设计的试验室制备干燥Cl2的实验装置图,根据图中的装置和有关试剂回答下列问题:
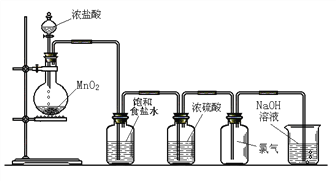
(1)该实验中还缺少一种仪器,这种仪器是_____________;
(2)饱和食盐水的作用是____________________;
(3)氯气与冷的氢氧化钠溶液反应生成NaCl、NaClO和H2O,与热的氢氧化钠溶液按照下面的反应进行:____________________
Cl2+ NaOH(热) - NaCl+ NaClO3+ H2O,请配平上述反应方程式;
(4)8.7 g MnO2和足量的浓盐酸反应,其中被氧化的HCl的物质的量为_________mol。
Ⅱ.某同学为探究铜跟浓硫酸的反应情况,用如图所示装置进行了有关实验。
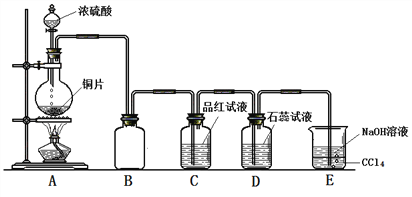
(1)B是用来收集实验中生成的气体的装置,但未将导管画全,请把导管补充完整_____________;
(2)D中的现象是_____________________;
(3)E中NaOH溶液的作用是_________________;
(4)下列药品中能够用来验证反应停止后的烧瓶中有H2SO4剩余的是__________(填字母编号)。
a.BaCl2溶液 b.NaHCO3粉末 c.Ba(NO3)2溶液 d.银粉
【答案】酒精灯吸收Cl2中的HCl气体 3 Cl2+ 6 NaOH(热)![]() 5 NaCl+ 1 NaClO3+ 3 H2O0.2
5 NaCl+ 1 NaClO3+ 3 H2O0.2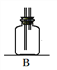 石蕊试液变红吸收SO2,防止污染空气b
石蕊试液变红吸收SO2,防止污染空气b
【解析】Ⅰ.(1)实验室制取氯气,常温下不能发生,需要加热,根据装置图,在制取装置中,缺少加热用的酒精灯.答案:酒精灯
(2)制取氯气使用浓盐酸,并且需要加热,会挥发出氯化氢气体,可用饱和食盐水,既吸收氯化氢,又降低氯气在水中的溶解度,饱和食盐水的作用是:吸收Cl2中的HCl气体,答案:吸收Cl2中的HCl气体
(3)Cl元素是变价元素,左边的Cl是0价,右边的NaCl中的Cl是-1,NaClO3中的Cl是+5,要升价和降价等同,那么就要有5个-1价的Cl元素和一个+5价的Cl,这样升价和降价才能平等,,配平了Cl元素,其它的都根据Cl元素既可。配平好的方程式为: 3 Cl2+ 6 NaOH(热)![]() 5 NaCl+ 1 NaClO3+ 3 H2O ,答案: 3 Cl2+ 6 NaOH(热)
5 NaCl+ 1 NaClO3+ 3 H2O ,答案: 3 Cl2+ 6 NaOH(热)![]() 5 NaCl+ 1 NaClO3+ 3 H2O ;
5 NaCl+ 1 NaClO3+ 3 H2O ;
(4)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,
MnCl2+Cl2↑+2H2O,
87g 4mol
8.7g 0.4mol
反应中参加反应的HCl为0.4 mol,其中被氧化的HCl为1/2×0.4=0.2 mol,另外的一半盐酸显酸性与Mn2+结合了,故其中被氧化的HCl的物质的量为0.2 mol,答案:0.2