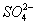题目内容
用光洁铂丝蘸取某无色溶液,在无色火焰上灼烧,火焰呈黄色,则无色溶液中
| A.只有Na+ | B.一定有Na+,可能有K+ |
| C.一定有Na+和K+ | D.可能有Na+和K+ |
B
试题分析:火焰呈黄色,说明该黄色归属于Na+,K+的焰色反应呈现出蓝色,当溶液中含有Na+和K+两种离子时,K+的蓝色常常被Na+掩盖,此时采用蓝色钴玻璃可以过滤掉Na+的黄色,所以该无色溶液一定有Na+,可能有K+,故本题的答案选B。
点评:本题考查了焰色反应的基本应用,钠和钾的焰色对于学生来说是比较熟悉的,所以本题难度不大。

练习册系列答案
相关题目
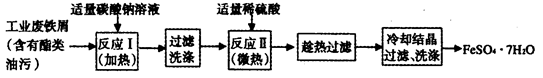
 +8H+=5Fe3++Mn2++4H2O),步骤为:
+8H+=5Fe3++Mn2++4H2O),步骤为: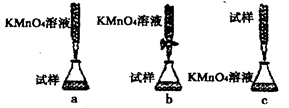
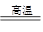 Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。
Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。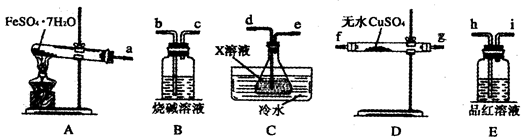
 中少量的
中少量的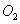 ,可将混合气体通过灼热的
,可将混合气体通过灼热的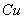 网
网
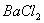 溶液有白色沉淀,该溶液中一定含有
溶液有白色沉淀,该溶液中一定含有