题目内容
7. 碳是地球上含量丰富的元素,其氧化物的研究有着重要意义.
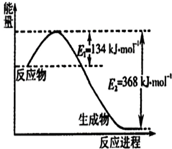
碳是地球上含量丰富的元素,其氧化物的研究有着重要意义.(1)如图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ/mol.
(2)试在原图基础上画出加入正催化剂后该反应在反应过程中的能量变化示意图(进行必要的标注).
分析 (1)由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368-134=234kJ,根据热化学方程式书写原则进行书写;
(2)加入催化剂,降低反应物的活化能,反应速率加快.
解答 解:(1)由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368-134=234kJ,反应热化学方程式为NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ/mol,
故答案为:NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ/mol;
(2)加入催化剂,降低反应物的活化能,反应速率加快,图象应为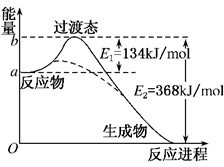 ,
,
故答案为: .
.
点评 本题考查反应热的有关计算以及催化剂对反应活化能的影响,题目难度中等,注意热化学方程式的计算以及加入催化剂,降低反应物的活化能.

练习册系列答案
相关题目
18.下表列出了A~R9种元素在周期表中的位置
用元素符号填写下空:
(1)化学性质最不活泼的元素是Ar
(2)这9中元素中金属性最强的是K
(3)A在F中燃烧得到产物的化学式Na2O2
(4)G的最高价含氧酸的化学式是HCl04
(5)C与D的原子半径比较:R(D)< R(C)(填“>”或“<”)
(6)E的最简单氢化物的化学式CH4.
| 周期 族 | IA | ⅡA | ⅢA | ⅣA | VA | VIA | VⅡA | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
(1)化学性质最不活泼的元素是Ar
(2)这9中元素中金属性最强的是K
(3)A在F中燃烧得到产物的化学式Na2O2
(4)G的最高价含氧酸的化学式是HCl04
(5)C与D的原子半径比较:R(D)< R(C)(填“>”或“<”)
(6)E的最简单氢化物的化学式CH4.
2.下列说法正确的是( )
| A. | 人们常借助元素分析仪来确定有机化合物的组成 | |
| B. | 有机化合物的核磁共振氢谱可以帮助我们确定物质中氢原子的种类 | |
| C. | 根据对红外光谱的分析,可以初步判定该有机物中碳原子的种类 | |
| D. | 用质谱法对有机物进行分析,可以初步判断该有机物中具有哪些基团 |
12.如表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题.
(1)元素④在周期表中所处位置第二周期ⅥA族⑤、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是P3->S2->Na+.
(2)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:PH3<H2S<H2O(写氢化物的化学式).
(3)元素⑦的原子结构示意图是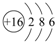 .
.
(4)用电子式表示①与⑨反应得到的化合物的形成过程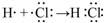 .
.
| ⅠA | ⅧA | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑧ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ | ||||
(1)元素④在周期表中所处位置第二周期ⅥA族⑤、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是P3->S2->Na+.
(2)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:PH3<H2S<H2O(写氢化物的化学式).
(3)元素⑦的原子结构示意图是
 .
.(4)用电子式表示①与⑨反应得到的化合物的形成过程
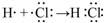 .
.
19.电负性的大小也可以作为判断元素金属性和非金属性强弱的尺度.下列关于电负性的变化规律正确的是( )
| A. | 周期表从左到右,元素的电负性逐渐变大 | |
| B. | 周期表从上到下,元素的电负性逐渐变大 | |
| C. | 电负性越大,金属性越强 | |
| D. | 电负性越小,非金属性越强 |
16.已知:C(s)+O2(g)=CO2(g)△H1
CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
4Fe(s)+3O2(g)=2Fe2O3(s)△H4
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
4Fe(s)+3O2(g)=2Fe2O3(s)△H4
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
| A. | △H1>0,△H3<0 | B. | △H2>0,△H4>0 | C. | △H2=△H1+△H3 | D. | △H3=$\frac{V{H}_{4}+2V{H}_{5}}{3}$ |
17.下列有机物的命名肯定错误的是( )
| A. | 3-甲基-2-戊烯 | B. | 3-甲基-2-丁烯 | C. | 2,2-二甲基丙烷 | D. | 2-甲基-1-丁炔 |
 .
.