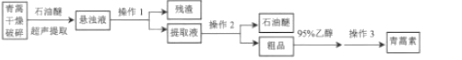
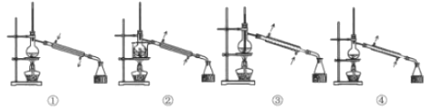
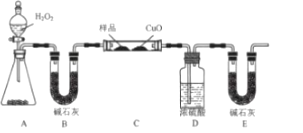
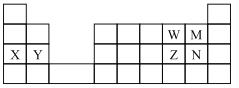
题目内容
【题目】化合物A经李比希法测得其中含C 72.0%、H 6.67%,其余为氧;质谱法分析得知A的相对分子质量为150。现代仪器分析有机化合物的分子结构有以下两种方法。
方法一:核磁共振仪测出A的核磁共振氢谱有5个峰,其面积之比为1∶2∶2∶2∶3。
方法二:利用红外光谱仪可初步检测有机化合物中的某些基团,现测得A分子的红外光谱如图:
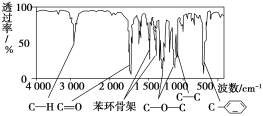
已知:A分子中只含一个苯环,且苯环上只有一个取代基。试回答下列问题。
(1)A的分子式为________。
(2)A的结构简式为_______________________________________________(写一种即可)。
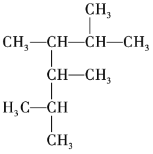
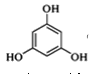
(3)A的芳香化合物类同分异构体有多种,其中分子中不含甲基的芳香酸为________。
【答案】C9H10O2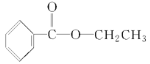 (或
(或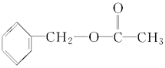 或
或 )
)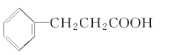
【解析】
(1)由相对分子质量及C、H、O的比例可得出A的分子式。N(C)=![]() =9,N(H)=
=9,N(H)=![]() ≈10,N(O)=
≈10,N(O)=![]() ≈2,所以分子式为C9H10O2,故答案为:C9H10O2;
≈2,所以分子式为C9H10O2,故答案为:C9H10O2;
(2)由核磁共振氢谱可知,A分子中含有五种氢原子,原子个数分别为1、2、2、2、3。由红外光谱可知分子中有C—H、C===O、C—O—C、C—C、![]() 结构。由已知信息苯环上只有一个取代基,可知苯环上的5个氢原子分成了三种,个数分别为1、2、2,另外5个氢原子分成两种,个数分别是2、3,取代基上3个C,5个H,再结合此分子的红外光谱可知,分子中有酯基,可得A的结构简式为
结构。由已知信息苯环上只有一个取代基,可知苯环上的5个氢原子分成了三种,个数分别为1、2、2,另外5个氢原子分成两种,个数分别是2、3,取代基上3个C,5个H,再结合此分子的红外光谱可知,分子中有酯基,可得A的结构简式为 、
、 或
或 ,故答案为:
,故答案为: (或
(或 或
或 );
);
(3)A的芳香化合物类同分异构体有多种,其中分子中不含甲基的芳香酸为![]() ,故答案为:
,故答案为:![]() 。
。

【题目】工业上常用绿柱石(主要成分3BeOAl2O36SiO2,还含有铁元素)冶炼铍,其简化的工艺流程如图所示:
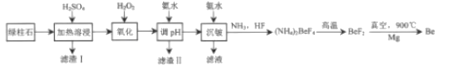
已知:Be和Al性质相似:几种金属阳离子的氢氧化物沉淀时的pH如表:
Be2+ | Al3+ | Fe3+ | Fe2+ | |
开始沉淀时 | 5.2 | 3.3 | 1.5 | 6.5 |
沉淀完全时 | 8.8 | 5.0 | 3.7 | 9.7 |
回答下列问题:
(1)滤渣Ⅰ的主要成分是______,加入H2O2的作用是______。
(2)得到滤渣Ⅱ的合理pH范围是______。
(3)用化学方程式解释不宜使用NaOH溶液来沉铍的原因是______。
(4)得到(NH4)2BeF4的化学方程式为______。
(5)由Mg还原BeF2得到Be需要真空的环境,其原因是______。
(6)若绿柱石中BeO的含量为a%,1吨绿柱石能生产含铍2%的合金b吨,则Be的利用率为______。(用含a、b的表达式表示)