题目内容
【题目】两种金属接触时,接触部位会发生“电偶腐蚀”。金属铁和铜在自来水和海水中,相同时间发生的腐蚀情况如图。下列有关说法正确的是( )
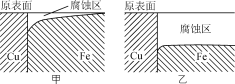
A.甲图中的介质为海水
B.腐蚀过程中电能转化为化学能
C.铁电极反应式为Fe-3e-=Fe3+
D.若在金属表面涂油漆,可以减弱铁的腐蚀
【答案】D
【解析】
铁和铜接触时,遇到电解质溶液会形成原电池,且形成的原电池中铁作负极,铜作正极,电解质为海水时的腐蚀速度大于水作电解质时的腐蚀速度,因此甲图的介质为水,乙图的介质是海水,且腐蚀的过程中化学能转化为了电能,据此分析判断。
A. 由分析可知,甲图的介质为水,乙图的介质是海水,A项错误;
B. 腐蚀的过程中化学能转化为了电能,B项错误;
C. 形成的原电池中铁作负极,失去电子,电解反应为:Fe-2e-=Fe2+,C项错误;;
D. 在金属表面涂油漆,可以减弱铁的腐蚀,D项正确;
答案选D。

练习册系列答案
相关题目
【题目】PCl3和PCl5都是重要的化工原料。将PCl3(g)和Cl2(g)充入2L的恒容密闭容器中,在一定条件下发生反应PCl3(g)+Cl2(g)![]() PCl5(g),△H<0并于10min时达到平衡。有关数据如下:下列判断正确的是
PCl5(g),△H<0并于10min时达到平衡。有关数据如下:下列判断正确的是
PCl3(g) | Cl2(g) | PCl5(g) | |
初始浓度/(molL-1) | 2.0 | 1.0 | 0 |
平衡浓度/(molL-1) | c1 | c2 | 0.4 |
A.10min内,v(Cl2)=0.02mol/(Lmin)
B.升高温度,反应的平衡常数增大
C.反应达到平衡时容器内的压强与初始时容器的压强之比为1:2
D.平衡后移走2.0molPCl3和1.0molCl2,相同条件下再达平衡时,c(PCl5)<0.2molL-1