题目内容
下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据。
| 元素 | I1/eV | I2/eV | I3/eV[ |
| 甲 | 5.7 | 47.4 | 71.8 |
| 乙 | 7.7 | 15.1 | 80.3 |
| 丙 | 13.0 | 23.9 | 40.0 |
| 丁 | 15.7 | 27.6 | 40.7 |
根据以上数据分析,下列说法正确的是
A.甲的金属性比乙弱 B.乙的化合价为+1价
C.丙一定为非金属元素 D.丁一定为金属元素
C
解析试题分析:根据电离能数据可知,甲元素的第二电离能远大于第一电离能,因此甲是第IA族元素。乙元素的第三电离能远大于第二电离能,所以乙元素是第ⅡA族元素。丙和丁的第一电离能均大于甲和乙的第一电离能,且二者的其余电离能相差不大,这说明二者一定不是ⅢA族元素。由于同周期自左向右非金属性逐渐增强,所以二者都是非金属。A、甲的金属性强于乙的金属性,A不正确;B、乙的化合价是+2价,B不正确;丙和丁都是非金属,C正确,D不正确,答案选C。
考点:考查元素电离能的判断和应用

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
六种短周期元素(a、b、c、d、e、f)的原子序数依次增大。其中a与e同主族,b与f同主族,e与f同周期;常温下a、e的单质状态不同;d的核电荷数是b的最外层电子数的2倍;单质f是一种重要的半导体材料。由此可推知
| A.a、c两种元素只能组成化学式为ca3的化合物 |
| B.b、c、d分别与a形成的化合物,沸点由高到低依次为:d>c>b |
| C.原子半径由大到小的顺序是 e>f>b>c>a |
| D.元素的非金属性由强到弱的顺序是 d>c>f>b |
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是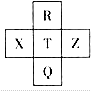
| A.非金属性:Z>T>X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R<T<Q |
| D.R、T、Q的最高正价相同 |
若某一个原子在处于能量最低状态时,外围电子排布为4d15s2,则下列各项说法正确的是
| A.该元素原子最外层共有3个电子 |
| B.该元素位于第5周期ⅡA族 |
| C.该元素原子核外第N层上共有9个不同状态的电子 |
| D.该元素原子第四电子层上有5个空轨道 |
原子序数在3~9之间的元素,随着核电荷数的递增而逐渐增大的是
| A.电子层数 | B.最外层电子数 | C.原子半径 | D.化合价 |
下列关于氢原子电子云图的说法正确的是
| A.通常用小黑点来表示电子的多少,黑点密度大,电子数目大 |
| B.黑点密度大,单位体积内电子出现的机会大 |
| C.通常用小黑点来表示电子绕核作高速圆周运动 |
| D.电子云图是对电子运动无规律性的描述 |