题目内容
温度不变,在恒容的容器中进行下列反应:N2O4(g) 2NO2(g),若N2O4的浓度由0.1 mol· L-1降到0.07 mol· L-1需要15 s,那么N2O4的浓度由0.07 mol·L-1降到0.05 mol·L-1所需反应的时间( )
2NO2(g),若N2O4的浓度由0.1 mol· L-1降到0.07 mol· L-1需要15 s,那么N2O4的浓度由0.07 mol·L-1降到0.05 mol·L-1所需反应的时间( )
 2NO2(g),若N2O4的浓度由0.1 mol· L-1降到0.07 mol· L-1需要15 s,那么N2O4的浓度由0.07 mol·L-1降到0.05 mol·L-1所需反应的时间( )
2NO2(g),若N2O4的浓度由0.1 mol· L-1降到0.07 mol· L-1需要15 s,那么N2O4的浓度由0.07 mol·L-1降到0.05 mol·L-1所需反应的时间( )| A.大于10 s | B.等于10 s | C.等于5 s | D.小于10 s |
A
试题分析:设需要的时间是t。由于反应物的浓度是逐渐降低的,因此反应速率也是逐渐降低的,即(0.1mol/L-0.07mol/L)÷15s>(0.07mol/L-0.05mol/L)÷t,解得t>10s,答案选A
点评:该题的关键是依据反应物浓度的降低,得出反应速率逐渐降低这一结论,然后列出相应的关系式计算加快。

练习册系列答案
相关题目

 (正)_____________
(正)_____________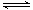 2SO3(g)。达平衡时测得有关数据如下表:
2SO3(g)。达平衡时测得有关数据如下表: (g)+5
(g)+5 (g)
(g) 4NO(g)+6
4NO(g)+6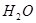 (g)在10L密闭容器中进行,
(g)在10L密闭容器中进行, (NH3)="0.0100" mol·L-1·S-1
(NH3)="0.0100" mol·L-1·S-1 4NO+6H2O,若反应速率分别用
4NO+6H2O,若反应速率分别用 、
、 、
、 、
、 [(mol / (L·min)]表示,则正确的关系是 ( )
[(mol / (L·min)]表示,则正确的关系是 ( )  3B(g)+C(g),若反应物在前20s由3mol降为1.8mol,则前20s的平均反应速率为
3B(g)+C(g),若反应物在前20s由3mol降为1.8mol,则前20s的平均反应速率为 pC(g)+qD(g)在一密闭容器中进行,测得平均反应速率υ(C)=2υ(B),且反应前后容器内的压强不变,则m、n、p、q的数值是( )
pC(g)+qD(g)在一密闭容器中进行,测得平均反应速率υ(C)=2υ(B),且反应前后容器内的压强不变,则m、n、p、q的数值是( ) C
C