��Ŀ����
һ���¶��£��ݻ�Ϊ2 L�ļס������̶��ݻ����ܱ������У�������Ӧ�� 2SO2(g)��O2(g)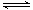 2SO3(g)����ƽ��ʱ����й��������±���
2SO3(g)����ƽ��ʱ����й��������±���
����˵����ȷ����( )
A����1+��2>1
B��1.6<a<3.2
C�������з�Ӧ2 minʱ�ﵽƽ�⣬��2 min ��ƽ��������(O2)=" 0.2" mol��L��1��min-1
D����ƽ����ټ���0.2 mol SO2��0.2 mol O2��0.4 mol SO3��ƽ�������ƶ�
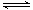 2SO3(g)����ƽ��ʱ����й��������±���
2SO3(g)����ƽ��ʱ����й��������±���| �� �� | �� | �� |
| ��Ӧ��Ͷ���� | 2 mol SO2��1 mol O2 | 4 mol SO3 |
| n(SO3)/mol | 1.6 | a |
| ��Ӧ���ת���� | ��1 | ��2 |
A����1+��2>1
B��1.6<a<3.2
C�������з�Ӧ2 minʱ�ﵽƽ�⣬��2 min ��ƽ��������(O2)=" 0.2" mol��L��1��min-1
D����ƽ����ټ���0.2 mol SO2��0.2 mol O2��0.4 mol SO3��ƽ�������ƶ�
C
�������������:2SO2(g)��O2(g)
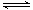 2SO3(g)
2SO3(g)ʼ(mol) 2 1
��(mol)1.6 0.8 1.6
ƽ(mol)0.4 0.2 1.6
��2min�ﵽƽ�⣬��2min��O2�ķ�Ӧ����Ϊ0.4mol/L/2min=0.2mol/(L��min)��C��ȷ������ƽ�ⳣ��Ϊ1600��ƽ������������ټ�0.2 mol SO2��0.2 mol O2��0.4 mol SO3����ʱQ=55.5<K��ƽ�������ƶ���D����
���� 2SO3(g)
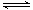 2SO2(g)��O2(g)
2SO2(g)��O2(g)ʼ(mol) 4
��(mol) 2x 2x x
ƽ(mol) 4-2x 2x x
�ס����ݻ��̶���������ʼʱͶ��4molSO3�൱��4molSO2��2molO2������2-x>1.6��x<0.4����1+��2<1��A����a>3.2��B����
������������Ȼ����ƽ�ⲻ��Ч�������Խ����Чƽ���֪ʶ����������ʼʱͶ��2molSO3������ƽ���Ч��

��ϰ��ϵ�д�
�����Ŀ
 2Y��g��+Z��g������YŨ����0.048mol��L��1���ӵ�0.12 mol��L��1��18s����ô����0.12mol��L��1���ӵ�0.2mol��L��1����Ҫ��Ӧ��ʱ����
2Y��g��+Z��g������YŨ����0.048mol��L��1���ӵ�0.12 mol��L��1��18s����ô����0.12mol��L��1���ӵ�0.2mol��L��1����Ҫ��Ӧ��ʱ���� 2SO3(g)����H<0��
2SO3(g)����H<0��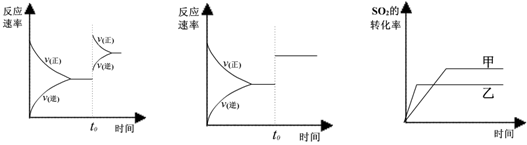
 ��
�� ��
�� ��ʾ����֪2
��ʾ����֪2 2NO2��g������N2O4��Ũ����0.1 mol�� L-1����0.07 mol�� L-1��Ҫ15 s����ôN2O4��Ũ����0.07 mol��L-1����0.05 mol��L-1���跴Ӧ��ʱ�䣨 ��
2NO2��g������N2O4��Ũ����0.1 mol�� L-1����0.07 mol�� L-1��Ҫ15 s����ôN2O4��Ũ����0.07 mol��L-1����0.05 mol��L-1���跴Ӧ��ʱ�䣨 �� 3C+4D�ķ�Ӧ�У������ò�ͬ���ʵı仯��ʾ�÷�Ӧ������������
3C+4D�ķ�Ӧ�У������ò�ͬ���ʵı仯��ʾ�÷�Ӧ������������