题目内容
在一定条件下,将 两种气体通入密闭容器中,反应按
两种气体通入密闭容器中,反应按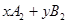 =
=  进行,
进行,
2秒钟后反应速率如下: ,
, ,
, ,则x、y的值分别为( )
,则x、y的值分别为( )
 两种气体通入密闭容器中,反应按
两种气体通入密闭容器中,反应按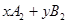 =
=  进行,
进行,2秒钟后反应速率如下:
 ,
, ,
, ,则x、y的值分别为( )
,则x、y的值分别为( )| A.3和2 | B.1和3 | C.3和1 | D.4和5 |
B
因为反应速率之比是相应的化学计量数之比,所以x和y之比是1︰3.答案选B。

练习册系列答案
相关题目
题目内容
 两种气体通入密闭容器中,反应按
两种气体通入密闭容器中,反应按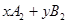 =
=  进行,
进行, ,
, ,
, ,则x、y的值分别为( )
,则x、y的值分别为( )| A.3和2 | B.1和3 | C.3和1 | D.4和5 |
