题目内容
11.下列各组物质中,化学键类型相同,晶体类型也相同的是( )| A. | NaCl和Mg | B. | NH4Cl和NH3 | C. | Cu和Hg | D. | CO2和SiO2 |
分析 根据晶体的类型和所含化学键的类型分析,离子化合物含有离子键,可能含有共价键,共价化合物只含共价键,双原子分子或多原子分子含有共价键.
解答 解:A、NaCl中钠离子和氯离子之间形成离子键和Mg是金属键,故A错误;
B、NH4Cl含有离子键和共价键和NH3中只含共价键,而氯化铵是离子晶体,氨气是分子晶体,故B错误;
C、Cu和Hg都由金属键形成的金属晶体,故C正确;
D、CO2和SiO2都是共价键形成,但二氧化碳是分子晶体而二氧化硅是原子晶体,故D错误;
故选:C.
点评 本题考察了化学键类型和晶体类型的关系.判断依据为:离子晶体中阴阳离子以离子键结合,原子晶体中原子以共价键结合,分子晶体中分子之间以范德华力结合,分子内部存在化学键.

练习册系列答案
相关题目
1.BF3与一定量的水形成(H2O)2•BF3晶体Q,Q在一定条件下可转化为R.反应过程中新形成的化学键中无( )


| A. | 离子键 | B. | 配位键 | C. | 金属键 | D. | 氢键 |
2.离子方程式中CO32-+2H+═H2O+CO2↑的CO32-不可能来自下列物质中的( )
| A. | K2CO3 | B. | Na2CO3 | C. | CaCO3 | D. | (NH4)2CO3 |
19.FeCl3溶液与下列物质的反应,其中与Fe3+的水解无关的一组是( )
①紫色石蕊试液
②碘化钾
③煮沸的蒸馏水
④硫化氢
⑤苯酚
⑥铜粉
⑦小苏打溶液
⑧镁粉.
①紫色石蕊试液
②碘化钾
③煮沸的蒸馏水
④硫化氢
⑤苯酚
⑥铜粉
⑦小苏打溶液
⑧镁粉.
| A. | ②④⑤⑥ | B. | ①②④ | C. | ③⑧ | D. | ②④⑧ |
6.在四个不同的容器中,在不同的条件下进行合成氨反应N2+3H2?2NH3,根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是( )
| A. | v(NH3)=0.3 mol/(L•min) | B. | v(N2)=0.01 mol/(L•s) | ||
| C. | v(N2)=0.2 mol/(L•min) | D. | v(H2)=0.3 mol/(L•min) |
16.能用H++OH-=H2O来表示的化学反应是( )
| A. | Ba(OH)2溶液滴入稀硫酸中 | B. | 氢氧化钠溶液和稀硝酸反应 | ||
| C. | 氢氧化镁和稀盐酸反应 | D. | NaOH溶液滴入醋酸中 |
3.只用一种试剂,可以一次性鉴别NH4Cl、NaCl、Na2SO4三种溶液,这种试剂是( )
| A. | Ba(OH)2溶液 | B. | KCl溶液 | C. | 酚酞溶液 | D. | 盐酸 |
20.下列说法错误的是( )
| A. | 从CH4、NH4+、SO42-为正四面体结构,可推测PH4-、PO43-也为正四面体结构 | |
| B. | 1 mol金刚石晶体中,平均含有2 mol C-C键 | |
| C. | HF、HCl、HBr、HI的热稳定性从左到右依次减弱 | |
| D. | 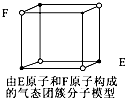 某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE |
1.下列应用与盐类的水解无关的是( )
| A. | 纯碱溶液可去除油污 | |
| B. | FeCl3饱和溶液滴入沸水中制Fe(OH)3胶体 | |
| C. | TiCl4溶于大量水加热制备TiO2 | |
| D. | 保存FeSO4溶液时加入少量铁粉 |