题目内容
3.下列有关化学用语正确的是( )| A. | 某元素基态原子的电子排布图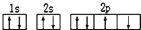 | |
| B. | NH4Cl电子式为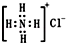 | |
| C. | Ca2+离子基态电子排布式为1s22s22p63s23p6 | |
| D. | 钾(K)的原子结构示意图为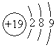 |
分析 A、2p的未成对电子自旋方向应该相同,能够最低进行判断;
B、氯离子电子式中电子没有表示出来;
C、根据构造原理判断钙离子的基态电子排布式;
D、根据构造原理判断钾原子的结构示意图.
解答 解:A、原子的电子排布图中,该元素2p的未成对电子自旋方向应该相同,正确为: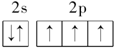 ,必须满足能量最低,故A错误;
,必须满足能量最低,故A错误;
B、氯化铵的电子式为: ,故B错误;
,故B错误;
C、根据构造原理,Ca2+离子基态电子排布式为:1s22s22p63s23p6,故C正确;
D、根据构造原理,钾原子的原子结构示意图为: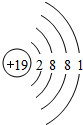 ,故D错误;
,故D错误;
故选C.
点评 本题考查了电子式、原子结构示意图等化学用语的表示方法,可以所学知识进行判断,本题难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.1mol某烃在氧气中充分燃烧,需要消耗氧气246.4L(标准状况下).它在光照的条件下与氯气反应能生成四种不同的一氯取代物.该烃的结构简式是( )
| A. | 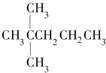 | B. | CH3CH2CH2CH2CH3 | C. | 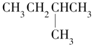 | D. | 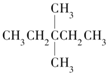 |
14. 氢气是新型能源和重要化工原料.
氢气是新型能源和重要化工原料.
已知:①2CO(g)+O2(g)=2CO2(g)△H1
②CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H2
③H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H2
(1)科学家提出一种利用天然气制备氢气的方法:CH4(g)+CO2(g)=2CO(g)+2H2(g)△H
△H=△H2-△H1-2△H3.这种方法的推广与使用,不仅实现资源综合利用,而且还能解决环境问题是.
(2)氨气是重要化工原料,在国民经济中占重要地位.
①在恒温、容积相等的恒容密闭容器中投入一定量氮气、氢气,发生如下可逆反应:
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1
实验测得起始、平衡时的有关数据如表所示:
下列判断正确的是BC.
A.N2的转化率:Ⅱ>I>Ⅲ
B.放出热量:a<b<92.4n
C.达到平衡时氨气的体积分数:Ⅲ>Ⅰ
D.平衡常数:Ⅲ>Ⅱ>Ⅰ
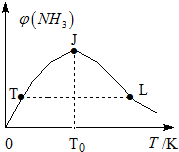
②在密闭恒容容器中投入一定量氮气和氢气,混合气体中氨气体积分数和温度关系如图所示:
曲线TJ段变化主要原因是,JL段变化的主要原因是.氨气正反应速率:T点小于 L点(填:大于、小于或等于).
③在2L密闭容器中充入一定量的氨气,氨气的物质的量与反应时间关系如表所示:
在该条件下,前5分钟H2平均反应速率为0.15mol•L-1•min-1.
④常温下,在V mL的a mol•L-1稀硫酸溶液中滴加b mol•L-1稀氨水V mL恰好使混合溶液呈中性.此时,一水合氨的电离常数Kb=$\frac{2a}{(b-2a)×107}$(用含a、b代数式表示).
(3)氢气直接作燃料电池的理论输出电压为1.2V,能量密度E=$\frac{\frac{1.2V×\frac{1000g}{2g/mol×2×96500C/mol}}{1kg}}{3.6×1{0}^{6}J•k{W}^{-1}•{h}^{-1}}$
=32.2kW•h•kg-1(列式计算).
 氢气是新型能源和重要化工原料.
氢气是新型能源和重要化工原料.已知:①2CO(g)+O2(g)=2CO2(g)△H1
②CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H2
③H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H2
(1)科学家提出一种利用天然气制备氢气的方法:CH4(g)+CO2(g)=2CO(g)+2H2(g)△H
△H=△H2-△H1-2△H3.这种方法的推广与使用,不仅实现资源综合利用,而且还能解决环境问题是.
(2)氨气是重要化工原料,在国民经济中占重要地位.
①在恒温、容积相等的恒容密闭容器中投入一定量氮气、氢气,发生如下可逆反应:
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1
实验测得起始、平衡时的有关数据如表所示:
| 容器编号 | 起始时各物质的物质的量/mol | 平衡时反应中的能量变化 | ||
| H2 | N2 | NH3 | ||
| Ⅰ | 3n | n | 0 | 放出热量a kJ |
| Ⅱ | 3n | 2n | 0 | 放出热量b kJ |
| Ⅲ | 6n | 2n | 0 | 放出热量c kJ |
A.N2的转化率:Ⅱ>I>Ⅲ
B.放出热量:a<b<92.4n
C.达到平衡时氨气的体积分数:Ⅲ>Ⅰ
D.平衡常数:Ⅲ>Ⅱ>Ⅰ
②在密闭恒容容器中投入一定量氮气和氢气,混合气体中氨气体积分数和温度关系如图所示:
曲线TJ段变化主要原因是,JL段变化的主要原因是.氨气正反应速率:T点小于 L点(填:大于、小于或等于).
③在2L密闭容器中充入一定量的氨气,氨气的物质的量与反应时间关系如表所示:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | … |
| NH3/mol | 2 | 1.0 | 0.5 | 0.25 | 0.24 | 0.24 |
④常温下,在V mL的a mol•L-1稀硫酸溶液中滴加b mol•L-1稀氨水V mL恰好使混合溶液呈中性.此时,一水合氨的电离常数Kb=$\frac{2a}{(b-2a)×107}$(用含a、b代数式表示).
(3)氢气直接作燃料电池的理论输出电压为1.2V,能量密度E=$\frac{\frac{1.2V×\frac{1000g}{2g/mol×2×96500C/mol}}{1kg}}{3.6×1{0}^{6}J•k{W}^{-1}•{h}^{-1}}$
=32.2kW•h•kg-1(列式计算).
11. 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实验条件,下列说法中一定不正确的是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实验条件,下列说法中一定不正确的是( )
 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实验条件,下列说法中一定不正确的是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实验条件,下列说法中一定不正确的是( ) | 组别 | 对应曲线 | c(HCl)/mol•L-1 | 反应温度/℃ | 铁的状态 |
| 1 | a | 30 | 粉末状 | |
| 2 | b | 30 | 粉末状 | |
| 3 | c | 2.5 | 块状 | |
| 4 | d | 2.5 | 30 | 块状 |
| A. | 第4组实验的反应速率最慢 | |
| B. | 第1组实验中盐酸的浓度大于2.5 mol•L-1 | |
| C. | 第2组实验中盐酸的浓度等于2.5 mol•L-1 | |
| D. | 第3组实验的反应温度低于30℃ |
18.下列过程中化学键没有被破坏的是( )
| A. | 水沸腾汽化 | B. | 水加热到1500℃开始分解 | ||
| C. | 熔融的氯化钠 | D. | NaOH溶于水 |
8.金刚石和石墨是碳元素的两种常见单质,下列叙述中正确的有 ( )
| A. | 金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化 | |
| B. | 晶体中共价键的键长:金刚石中C-C<石墨中C-C | |
| C. | 晶体的熔点:金刚石<石墨 | |
| D. | 晶体中共价键的键角:金刚石>石墨. |
12.主族元素在周期表中的位置取决于该元素原子的( )
| A. | 相对原子质量和核外电子数 | B. | 电子层数和最外层电子数 | ||
| C. | 相对原子质量和最外层电子数 | D. | 电子层数和次外层电子数 |
13.某元素构成的双原子单质分子有3种,其中相对分子量分别为158、160、162..在天然的单质中,这三种单质的物质的量之比为1;1:1,由此推断以下结论中,正确的是( )
| A. | 此元素有三种同位素 | |
| B. | 其中质量数为79的同位素原子占原子总数 $\frac{1}{2}$ | |
| C. | 其中一种同位素质量数为80 | |
| D. | 此元素单质的平均相对分子质量为160 |
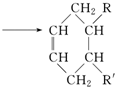 (可表示为
(可表示为 )其中,R、R′表示原子或原子团.
)其中,R、R′表示原子或原子团.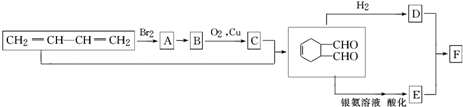
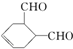 中官能团的名称是醛基.1mol该物质完全燃烧需消耗O26.5mol
中官能团的名称是醛基.1mol该物质完全燃烧需消耗O26.5mol .
.